2019-02-20 東京大学,日本医療研究開発機構
発表者
小林 修(東京大学大学院理学系研究科化学専攻 教授)
花田 賢太郎(国立感染症研究所細胞化学部 部長)
発表のポイント
- 細胞の中にあるさまざまな小器官(オルガネラ、注1)間でさまざまな脂質分子が移動しています。この細胞内脂質分子の物流は、多様な脂質輸送タンパク質群(注2)によって行われています。産官学連携により、セラミド輸送タンパク質CERT(注3)の新しい阻害剤を開発することに成功しました。
- ヒト細胞内には多様な脂質輸送タンパク質群が存在しますが、これら個々の脂質輸送タンパク質に特異的な阻害剤はまだありません。コレステロールを運ぶ輸送タンパク質の阻害剤は複数知られておりますが、それらはコレステロールに似た構造をもつため、コレステロールを結合する他のタンパク質にも作用してしまっていると考えられています。CERTに関しても、セラミドに類似した構造を持つ阻害剤HPA-12(注4)が20年近く前に開発されていますが、CERT以外でセラミドを結合する因子にも影響する可能性は残っています。今回、多角的アプローチを駆使して、セラミドとの構造類似性のない新規のCERT阻害剤HPCB-5を開発しました。
- 本研究成果は、さまざまな脂質輸送タンパク質を分子標的とした阻害剤開発の先駆けとなることが期待されます。
発表概要
東京大学大学院理学系研究科の小林修教授と、国立感染症研究所・細胞化学部の花田賢太郎部長を中心とした研究グループは、第一三共RDノバーレ株式会社所属研究員のグループとの産官学連携により、セラミド輸送タンパク質に対する新規阻害剤の開発に成功しました。
細胞の中にあるさまざまな小器官(オルガネラ)間の脂質の移動は多様な脂質輸送タンパク質群によって行われています。脂質輸送タンパク質群は細胞にとって重要なだけでなく、ウイルスのような細胞寄生性の病原体が増えることにも利用されています。しかし、脂質輸送タンパク質に対する特異的な阻害剤は開発されておりませんでした。小胞体からゴルジ体細胞内のセラミド輸送を担うセラミド輸送タンパク質CERTに関しては、セラミド類似構造をもつ阻害剤HPA-12が小林と花田らにより2001年に開発されておりましたが、今回、最新の技術を結集させながら、セラミドとの構造類似性のない新規のCERT阻害剤HPCB-5の開発に成功しました。構造的に全く異なる阻害剤セットは、CERT機能を特異的に抑止したときに起こる生物学的表現型を知るための優れた薬剤ツールになるだけでなく、さまざまな脂質輸送タンパク質を分子標的とした阻害剤開発の先駆けとなると期待できます。
本研究成果は、ネイチャー出版グループ(Nature Publication Group)の新オープンアクセスのオンライン雑誌「Communications Chemistry」で2月20日(現地時間)に公開されます。なお本研究は、国立研究開発法人日本医療研究開発機構の革新的先端研究開発支援事業(AMED-CREST)『画期的医薬品等の創出をめざす脂質の生理活性と機能の解明』領域(研究開発総括:横山信治)における研究開発課題「病原体による宿主脂質ハイジャック機序の解明と創薬への応用(研究代表者:花田賢太郎)」および文科科学省の新学術領域研究などの一環として行われました。
発表内容
研究の背景
全ての生き物の基本単位は細胞です。人間を含めた動物の細胞の中には小胞体、ゴルジ体、ミトコンドリアといったさまざまな小器官(オルガネラ)が常に存在していて、それぞれに割り当てられた働きを発揮しながら細胞を成り立たせています。オルガネラは膜に囲まれた構造体であり、その形成には脂質が過不足なく供給されなければならず、そのためのオルガネラ間の脂質分子の物流システムが存在しています。このオルガネラ間の脂質物流システムの主役は、多様な脂質輸送タンパク質群であることが近年わかってきました。また、ヒト細胞の脂質輸送タンパク質がウイルス等病原体の増殖に必要である例も複数報告されています。このような背景もあり、特定の脂質輸送タンパク質の働きを止めるような薬剤は新しい医薬品に結びつくと期待されています。しかし、数多くの脂質輸送タンパク質が発見されながら、その阻害剤はいままでほとんど開発されずにいました。既存の脂質輸送タンパク質阻害剤は、天然の脂質リガンドに似た構造を持っているため、その脂質を利用する他の分子にも作用するなど特異性においての問題が指摘されています。哺乳動物細胞の小胞体とゴルジ体の接触ゾーンでセラミドの輸送を行うセラミド輸送タンパク質 CERTの阻害剤としては、本研究グループが以前開発したセラミド類似構造を有する化合物HPA-12が、現時点で最も強力です。しかし、HPA-12はセラミドに類似した構造を持つため、セラミドをリガンドとする他の生体因子にも影響を及ぼすことが危惧されていました。
研究の内容
本研究グループは、定量的な親和性評価、コンピュータを用いたスクリーニング、効率的な有機化学合成、候補化合物との共結晶解析などの手法を用いた多角的アプローチを産官学連携により実施し、新たなCERT阻害剤を開発しました。新規化合物HPCB-5は、セラミド類似の化学構造は持たないものの(図1)、セラミド類似構造を有する既存CERT阻害剤と同等の親和性でCERTに結合しました。ヒト培養細胞投与時におけるHPCB-5のCERT阻害活性はHPA-12と同様に高く(図1)、HPCB-5が脂質代謝に与える影響はスフィンゴミエリン合成の抑制に限られているものの、スフィンゴミエリン合成酵素そのものは阻害しませんでした。細胞培養条件下での安定性はHPCB-5のほうがHPA-12よりもやや優れていました(図2)。これらの結果から、セラミドとの構造類似性はなくとも、HPCB-5は、セラミド類似構造を有するHPA-12と同様に、CERTに選択性のある阻害剤であり、細胞投与時の安定性はHPA-12よりも優れていることが明らかとなりました。
今後の展開
人工的化合物が目的とする生体分子以外にも結合して生物学的作用を発揮してしまうこと(いわゆるオフ・ターゲット効果)は、多寡はあれども全ての薬剤において避けられない問題です。薬剤投与の結果に起こることが、目的の標的への作用の結果なのか、オフ・ターゲット効果なのかを区別することは医薬開発では重要な事柄です。HPA-12とHPCB-5という構造的に全く異なる阻害剤のセットが揃ったことで、CERT機能を特異的に抑止したときに起こる生物学的表現型を知るための優れた薬剤ツールが提供できるようになると期待できます。すなわち、HPA-12とHPCB-5それぞれの投与で引き起こされる生物作用が似ている場合は、CERT阻害の結果として起こった現象であり、全く違っている場合はオフ・ターゲット効果による現象と評価できるでしょう。CERTが恒常的に活性化することで起こる先天性精神発育不全症の存在が最近報告され、そのような遺伝病の症状緩和・治療への道を本CERT阻害剤は開くかもしれません。また、将来的には宿主因子を分子標的とした抗感染症薬の候補にもなることが期待されます。
発表雑誌
- 雑誌名:
- 「Communications Chemistry」(オンライン版:2月20日)
- 論文タイトル:
- Natural ligand-nonmimetic inhibitors of the lipid-transfer protein CERT
- 著者:
- Naoki Nakao, Masaharu Ueno, Shota Sakai, Daichi Egawa, Hiroyuki Hanzawa, Shohei Kawasaki, Keigo Kumagai, Makoto Suzuki, Shu Kobayashi, and Kentaro Hanada
(N.N., M.U., and S.S. are the co-first authors. S.K. and K.H. are co-correspondence authors) - DOI番号:
- 10.1038/s42004-019-0118-3
用語解説
- 注1 オルガネラ
- 細胞の中には膜で囲まれたいろいろな種類の小器官(オルガネラ)が存在していて、それぞれに特有の機能を発揮して細胞を維持している。オルガネラの膜は主にタンパク質と脂質(リン脂質やコレステロール)から成り立っている。
- 注2 脂質輸送タンパク質
- 脂質は水に溶けないので、異なるオルガネラ膜の間で脂質分子が転移するには、タンパク質の助けが必要である。膜間の脂質の移動を助けるタンパク質を脂質輸送タンパク質と呼ぶ。ヒト細胞内には多くの種類の脂質輸送タンパク質が存在していている。
- 注3 セラミド輸送タンパク質CERT
- 小胞体で合成されたセラミド(注5)をスフィンゴミエリン(注6)の合成場であるゴルジ体へと運ぶ脂質輸送タンパク質である。CERTの活性が異常に亢進すると考えられるヒト遺伝子変異は精神発育不全の原因となる。また、ウイルスや細胞内寄生細菌のいくつかはCERTの機能を利用して増殖する。
- 注4 HPA-12
- CERTに対する既存の阻害剤。小林・花田らにより、セラミドに類似した構造を持つ新規化合物の中から2001年に開発された。生きたヒト細胞において効果のあることが実証されているCERT阻害剤としては最強であり、世界中の脂質研究の場で使用されている。
- 注5 セラミド
- セラミドは、皮膚に多い脂質として一般的には有名であるが、全てのヒト細胞に存在しており、スフィンゴミエリン、スフィンゴ糖脂質の合成前駆体になっている。セラミド合成のオルガネラである小胞体にセラミドが増えすぎると細胞死を招くと示唆されており、この現象を抗がん治療に応用しようとする研究も行われている。
- 注6 スフィンゴミエリン
- スフィンゴシンという構造を持つ脂質をスフィンゴ脂質と呼び、セラミド、スフィンゴミエリン、スフィンゴ糖脂質といったスフィンゴ脂質はどのヒト細胞にも普遍的に存在していて、細胞に不可欠な役割を果たしている。
添付資料
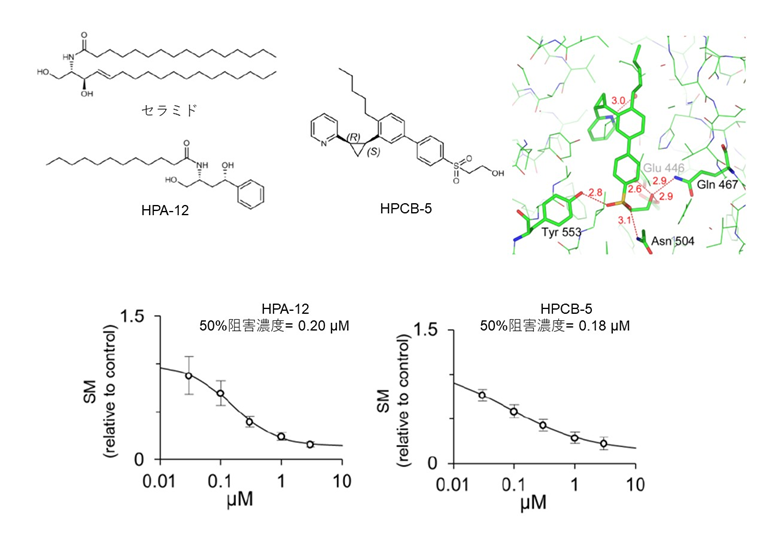
図1 天然型セラミド、既存のCERT阻害剤HPA-12及び新規に開発した阻害剤HPCB-5の化学構造。CERTに結合したHPCB-5の結晶構造も図示した。HPA-12とHPCB-5との間に化学構造上の類似点はほぼ無いが、ヒト培養細胞であるヒーラ細胞に投与すると同じようにCERTを阻害する。
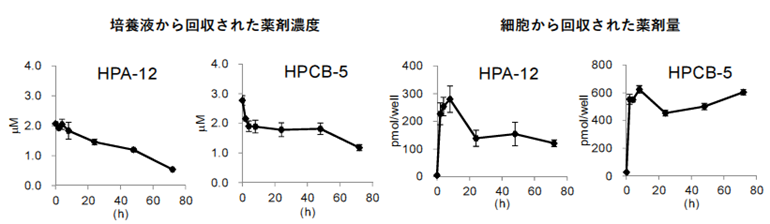
図2 12穴の細胞培養プレートにヒーラ細胞を播き、培養液に3µM のHPA-12または HPCB-5を添加して37°Cで培養した。図示した時間の後に培養液と細胞をそれぞれ回収し、含まれる薬剤量を質量分析法により定量した。培養液、細胞ともにHPCB-5のほうがHPA-12よりも量の減り方が緩やかであることから、細胞培養条件下での安定性はHPCB-5のほうが優れていると考えられる。
問い合わせ先
研究に関すること
東京大学大学院理学系研究科化学専攻
教授 小林 修(コバヤシ シュウ)
国立感染症研究所細胞化学部
部長 花田 賢太郎(ハナダ ケンタロウ)
報道に関すること
東京大学 大学院理学系研究科・理学部
特任専門職員 武田加奈子、教授・広報室長 大越慎一
AMED事業に関するお問い合わせ先
国立研究開発法人日本医療研究開発機構(AMED)
基盤研究事業部 研究企画課