2019-08-07 京都大学
ユーリー・ホン 高等研究院物質–細胞統合システム拠点(iCeMS=アイセムス)特定研究員(兼・理化学研究所客員研究員)、西山裕介 理化学研究所ユニットリーダー、山崎俊夫 同チームリーダー、米倉功治 同グループディレクター、日本電子株式会社らの研究グループは、100ナノメートル(nm、ナノは10億分の1)から1マイクロメートル(μm、マイクロは100万分の1)の大きさの微結晶を用いて、低分子有機化合物の水素原子の位置も含めた結晶構造を詳細に観測する手法を開発しました。
結晶構造解析法の単結晶X線回折では、10μm以上の単結晶が必要であり、製剤に含まれる低分子有効成分の微結晶(0.1から1μm程度)からは構造解析ができませんでした。
今回、本研究グループは、電子回折による全体構造解析と固体核磁気共鳴(固体NMR)による局所構造解析を、第一原理量子化学計算を用いて統合することで、0.1から1μmの微結晶から精密な構造解析ができる手法を開発しました。この手法では、一般の製剤に見られるような混ざり物があっても解析ができ、これまで構造が未知であった医薬品シメチジン(結晶形B)の構造解析にも成功しました。
本研究成果は、生活習慣病や花粉症などの低分子医薬品の開発促進や品質向上に貢献することが期待されます。
本研究成果は、2019年8月6日に、国際学術誌「Nature Communications」のオンライン版に掲載されました。
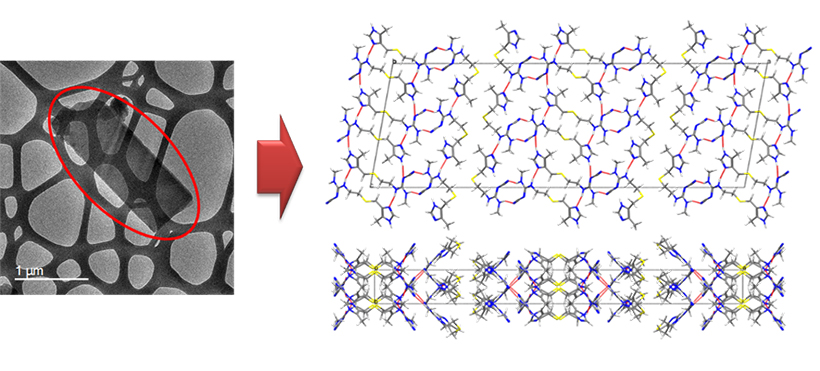 図:シメチジン結晶形Bの微結晶(左:赤丸内)から原子レベルの構造を解明
図:シメチジン結晶形Bの微結晶(左:赤丸内)から原子レベルの構造を解明
書誌情報
【DOI】 https://doi.org/10.1038/s41467-019-11469-2
【KURENAIアクセスURL】 http://hdl.handle.net/2433/243258
Candelaria Guzmán-Afonso, You-lee Hong, Henri Colaux, Hirofumi Iijima, Akihiro Saitow, Takuma Fukumura, Yoshitaka Aoyama, Souhei Motoki, Tetsuo Oikawa, Toshio Yamazaki, Koji Yonekura & Yusuke Nishiyama (2019). Understanding hydrogen-bonding structures of molecular crystals via electron and NMR nanocrystallography. Nature Communications, 10:3537.
詳しい研究内容について
ナノ結晶から水素結合を可視化
-低分子医薬品の開発促進や品質向上に期待-
理化学研究所(理研)科技ハブ産連本部バトンゾーン研究推進プログラム理研 -JEOL 連携センター[1]ナノ結晶解析連携ユニットの西山裕介ユニットリーダー (放射光科学研究センター NMR 応用・利用グループ 副グループディレクター、 株式会社 JEOL RESONANCE 技術部エキスパート)、放射光科学研究センター次 世代 NMR 装置開発チームの山崎俊夫チームリーダー、生体機構研究グループの 米倉功治グループディレクター、京都大学 iCeMS、日本電子株式会社らの共同研 究グループ※は、100 ナノメートル(nm、1nm は 10 億分の 1 メートル)~1 マ イクロメートル(μm、1μm は 100 万分の 1 メートル)の大きさの微結晶を用 いて、低分子有機化合物の水素原子の位置も含めた結晶構造を詳細に観測する 手法を開発しました。
本研究成果は、生活習慣病や花粉症などの低分子医薬品の開発促進や品質向 上に貢献すると期待できます。
結晶構造解析法の単結晶 X 線回折[2]では、10μm 以上の単結晶が必要であり、 製剤に含まれる低分子有効成分の微結晶(0.1~1μm 程度)からは構造解析がで きませんでした。
今回、共同研究グループは、電子回折[3]による全体構造解析と固体核磁気共鳴 (固体 NMR)[4]による局所構造解析を、第一原理量子化学計算[5]を用いて統合す ることで、0.1~1μm の微結晶から精密な構造解析ができる手法を開発しまし た。この手法では、一般の製剤に見られるような混ざり物があっても解析ができ、 これまで構造が未知であった医薬品シメチジン[6](結晶形 B)の構造解析にも成 功しました。
本研究は、英国のオンライン科学雑誌『Nature Communications』(8 月 6 日付 け:日本時間 8 月 6 日)に掲載されました。
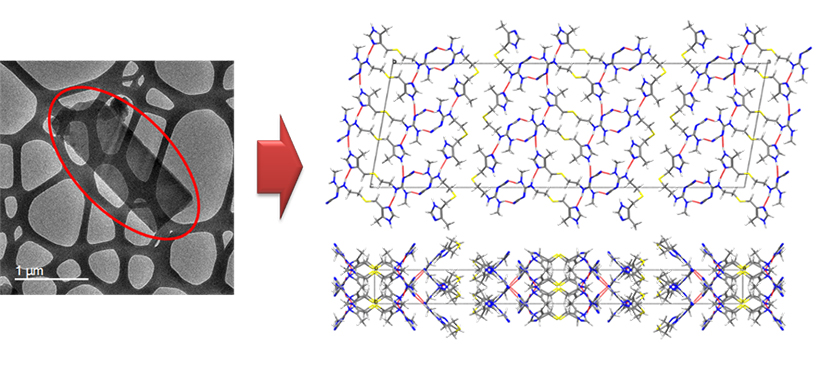 図 シメチジン結晶形 B の微結晶(左:赤丸内)から原子レベルの構造を解明
図 シメチジン結晶形 B の微結晶(左:赤丸内)から原子レベルの構造を解明
※共同研究グループ
理化学研究所
科技ハブ産連本部 バトンゾーン研究推進プログラム 理研-JEOL 連携センター
ナノ結晶解析連携ユニット
ユニットリーダー 西山 裕介 (にしやま ゆうすけ)
(放射光科学研究センター NMR 研究開発部門 NMR 応用・利用グループ 副グループディレクター、株式会社 JEOL RESONANCE 技術部エキスパート)
研究員(研究当時) カンデラリア・グズマン-アフォンソ (Candelaria Guzm n-Afonso)
客員研究員 ユーリー・ホン (You-lee Hong) (京都大学 iCeMS 特定研究員)
特別研究員(研究当時) アンリ・コロ(Henri Colaux)
放射光科学研究センター
NMR 研究開発部門 NMR 開発グループ 次世代 NMR 装置開発チーム チームリーダー 山崎 俊夫 (やまざき としお)
利用技術開拓研究部門 生体機構研究グループ グループディレクター 米倉 功治 (よねくら こうじ) (科技ハブ産連本部 バトンゾーン研究推進プログラム 理研-JEOL 連携センター 次世代電子顕微鏡開発連携ユニット ユニットリーダー)
日本電子株式会社 EM 事業ユニット
EM 第 1 技術開発部 第1グループ
主事 飯島 寛文 (いいじま ひろふみ)
EM 第 1 技術開発部 第 2 グループ
グループ長 齊藤 晃宏 (さいとう あきひろ)
EM アプリケーション部 Biology グループ 第 2 チーム
福村 拓真 (ふくむら たくま)
EM アプリケーション部 Material グループ 第 2 チーム
主事 青山 佳敬 (あおやま よしたか)
EM 第 1 技術開発部 第1グループ
グループ長 元木 創平 (もとき そうへい)
JEOL ASIA
シニアプロダクトマネージャー 及川 哲夫 (おいかわ てつお)
※研究支援
本研究は、日本学術振興会(JSPS)科学研究費補助金基盤研究 B「イオン駆動力供給 体の電子線と X 線による作動機構の解明(研究代表者:米倉功治)」、同挑戦的萌芽研究 「電子線結晶構造解析によるクーロンポテンシャルの可視化(研究代表者:米倉功治)」、 科学技術振興機構(JST)先端計測分析技術・機器開発プログラム「電子顕微鏡の高精 度制御及び生体高分子結晶構造解析ソフトウェアの開発(研究代表者:米倉功治)」な どの支援を受けて行われました。
1.背景
生活習慣病や花粉症などの治療には、長期保管や経口投与のできる低分子医 薬品が使われます。低分子医薬品の安定した薬効を保証するためには、含まれる 有効成分の結晶構造を管理することが重要です。特に、低分子有機化合物は同じ 化学式であっても、複数の結晶構造(結晶多形)や溶媒和物(結晶擬多形)の構 造をとりえます。結晶構造が異なると、それぞれの溶解度や安定度などが異なる ため薬効も変化します。
通常、製剤における結晶構造は、粉末 X 線回折[2]や固体核磁気共鳴(固体 NMR) を用いて決定されます。しかし、製剤には有効成分だけでなく、でんぷんや糖な どの賦形剤[7]が含まれているため、その X 線回折パターンや NMR スペクトルは、 有効成分と賦形剤からの信号が重なり合った複雑なものとなります。また、もし 製剤中に未知の結晶構造が存在していた場合は、その存在を検出することはで きません。たとえば、鎮痛剤として用いられるインドメタシンとカフェインの未 知の共結晶が市販の製剤中に観測された例が挙げられます。この共結晶は、イン ドメタシンとカフェインを粉末状態ですり合わせることで生成されますが、元 のそれぞれの結晶とは溶解性が異なるため、薬効が異なることが分かりました。 結晶をすり合わせるというプロセスは、製剤の過程でよく用いられるものです。 このような理由から、製剤中の有効成分の結晶構造を直接決定する技術が強く 求められています。
しかしながら、結晶構造の決定法として広く用いられている単結晶 X 線回折 では、少なくとも 10 マイクロメートル(μm、1μm は 100 万分の 1 メートル) 程度の単結晶が必要であり、製剤に含まれる 100 ナノメートル(nm、1nm は 10 億分の 1 メートル)~1μm(0.1~1μm)程度の低分子有機化合物の有効成分の 微結晶から結晶構造を直接決定することはできません。また、微結晶粉末試料か らの構造解析法として用いられている粉末 X 線回折は、単一成分からなる粉末 試料を要求し、混ざり物である製剤から直接構造を決定することはできません。
一方、電子回折で用いられる電子線と物質の相互作用は X 線と比べると 1~ 10 万倍程度も強いため、0.1~1μm 程度の微結晶からでも十分な回折パターン を得ることができます。そこで、ごく最近になり、電子回折を用いた低分子医薬 品の構造解析も報告され、注目を集めています。しかし、電子回折では、炭素、 窒素、酸素といった原子番号の近い原子を取り違えることが多く、さらに医薬品 中の水素結合を理解するのに重要な水素がはっきりと見えないといった問題が あります。
2.研究手法と成果
共同研究グループは、透過型電子顕微鏡[8]を用いた電子回折による全体構造解 析と固体 NMR による局所解析とを第一原理量子化学計算により統合させること で、0.1~1μm 程度の低分子有機化合物の微結晶から、結晶構造、水素結合構造 を正しく解明する手法を開発しました。
この手法ではまず、電子回折により大まかな結晶構造を調べますが、水素が見 えないことのほか、炭素・窒素・酸素が区別できないことから、複数の異性体が 構造候補として挙がります。そこで、これら異性体の固体 NMR スペクトルを、 第一原理量子化学計算を用いて計算します。この計算 NMR スペクトルと、実測 の固体 NMR スペクトルを比較することにより、どの異性体が正しい構造かを明 瞭に決定できます。
具体例として、構造が既知のアミノ酸 L-ヒスチジンの微結晶の場合、電子回 折を用いて構造解析を行うと(図 1)、分子構造上、炭素・窒素・酸素原子が全 く異なる帰属となっており、また水素原子の数や位置がでたらめになっている ことが分かります。また、分子構造の知見に加え、固体 NMR の測定結果によっ て訂正した構造(図 2)であってもなお四つの構造の可能性があります。そこで、 計算 NMR スペクトルと固体 NMR スペクトルを比較することにより、一つの構造 に絞り込めます(図 3)。
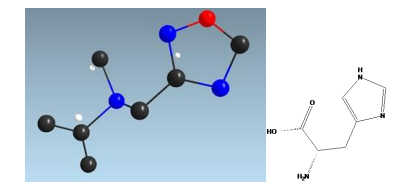
図1 L-ヒスチジンの構造式と電子回折を用いて得られた初期構造
黒が炭素、青が窒素、赤が酸素、白が水素を示す。ヒスチジンの化学式は C6H9N3O2だが、構造式と比較す るとそれぞれの原子の帰属が全く異なることが分かる。
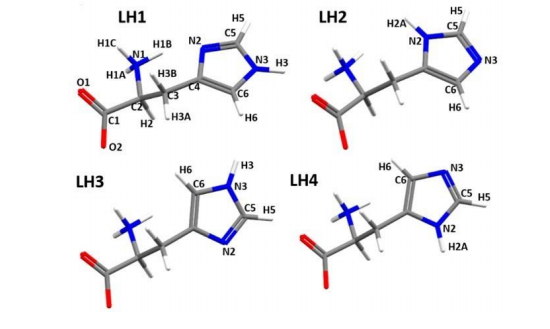
図 2 固体 NMR の測定結果から絞り込んだ四つの構造
側鎖のイミダゾイル基(5 員環の部分)が異なる四つの異性体に絞り込まれた。
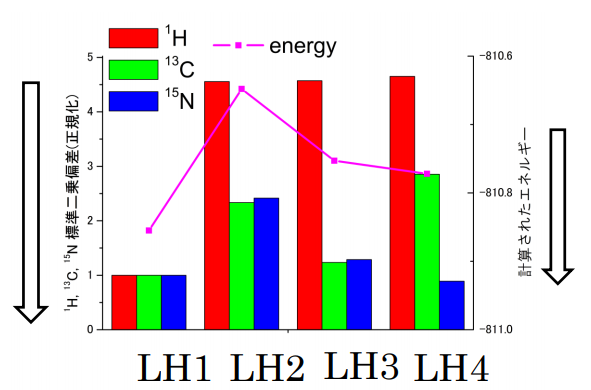
図 3 実側と計算 NMR スペクトルの比較と計算で得られたエネルギー
棒グラフは、実験で得られた固体 NMR スペクトルと量子化学計算で得られた NMR スペクトルの平均二乗 偏差を示す(左軸)。平均二乗偏差が小さいほど、二つのスペクトルが近いことを示す。紫の折れ線グラフ は、量子化学計算で得られた結晶格子のエネルギーで、エネルギーが小さいほど安定なことを示す(右軸)。 最も安定で最も実験 NMR スペクトルと一致することから、LH1 が正しい構造と決められた。
本手法を用いて、シメチジン結晶形 B [6]の構造決定を行いました。具体的には、 電子回折により大まかな構造決定を行い、結晶形 B と結晶形 C が混ざり合った 試料の中から類似の結晶パラメーターを持つ結晶からの電子回折データを集め ることで、結晶形 B の構造を決めることに成功しました。
今回の研究成果により、電子回折による構造の不確かさを固体 NMR と第一原 理量子化学計算により補い、最終的に一つの構造を導き出しました。また、得ら れた結晶構造で分子内、分子間で複雑に水素結合している姿が見られ、シメチジ ン結晶形 B の安定化機構が明らかになりました(図 4)。

図 4 シメチジン結晶形 B の微結晶の電子顕微鏡像と得られた結晶構造
左は、シメチジン結晶形 B の電子顕微鏡写真。右は、左の赤丸内の、固体 NMR および電子回折、量子化学 計算により得られた結晶構造。青は窒素原子、黄は硫黄原子、灰色が炭素原子、白が水素原子を示してい る。結晶構造はオレンジ線で示される水素結合により安定化されている。右下は、右上の構造を真横から 見たもの。
3.今後の期待
今回の研究成果では、電子回折と固体 NMR とを第一原理量子化学計算を通じ て有機的に結合することで、ナノサイズの微小な結晶から水素の位置も含めた 精密な結晶構造解析が実現しました。本手法の混合物であっても解析ができる 特徴を生かし、医薬品への応用が期待できます。低分子医薬品の精密な結晶構造 が、錠剤や散剤などの状態で決定できるため、今後、より安定した品質保証に貢 献することが考えられます。また、これまで見逃されてきた未知の結晶形の発見 も期待できることから、医薬品の改善にもつながります。
このほか、医薬品だけでなく微結晶試料一般への応用が考えられます。例えば、 ガス吸着・貯蔵・イオン伝導体などさまざまな構造機能化学材料として有望視さ れ、盛んに研究されている多孔性金属錯体(PCP/MOF)[9]が挙げられます。結晶 性が高い PCP/MOC は容易に微結晶試料が得られることから、本手法を適用する ことで、研究開発が加速すると期待できます。
4.論文情報
<タイトル>
Understanding hydrogen-bonding structures of molecular crystals via electron and NMR nanocrystallography
<著者名>
Candelaria Guzm n-Afonso†, You-lee Hong†, Henri Colaux, Hirofumi Iijima, Akihiro Saitow, Takuma Fukumura, Yoshitaka Aoyama, Souhei Motoki, Tetsuo Oikawa, Toshio Yamazaki, Koji Yonekura, Yusuke Nishiyama †These authors contributed equally to this work
<雑誌>
Nature Communications
<DOI>
10.1038/s41467-019-11469-2
5.補足説明
[1] 理研-JEOL 連携センター
理研と日本電子株式会社(JEOL)が共同で設立した連携センター。分析・診断機器分 野における独自技術の創出を目指し、2014 年 11 月に開設。 参考:2014 年 10 月 31 日トピックス「「理研 CLST-JEOL 連携センター」を開設」 http://www.riken.jp/pr/topics/2014/20141031_1/
[2] 単結晶 X 線回折、粉末 X 線回折
X 線回折とは、X 線を結晶に照射させて得られる X 線の散乱パターン(X 線回折像) から、結晶内の原子の配列の仕方(結晶構造)や電子の分布の仕方(電子密度分布) を決定する手法であり、試料に単結晶を用いる場合、単結晶 X 線回折と呼ばれる。試 料に単結晶の集合である粉末を用いる場合、粉末 X 線回折と呼ばれる。単結晶 X 線 回折は粉末 X 線回折に比べて、試料準備が困難、測定に時間がかかるなどのデメリッ トがある反面、回折ピークの重なりが少ない、回折強度が強いなどのメリットがある。
[3] 電子回折
結晶に電子線を照射して、散乱パターンを観測する手法。透過型電子顕微鏡を用いて 観測される。X 線回折では電子密度分布が得られるのに対して、電子回折では静電ポ テンシャルが得られる。X 線回折、中性子線回折と並ぶ回折手法の一つ。X 線や中性 子線と比べると、非常に小さい結晶から回折パターンが得られることが特徴。
[4] 固体核磁気共鳴(固体 NMR)法
原子核には核スピンがあり、これがゼロではない水素や炭素原子の一部は強い磁場の 中に置かれると、複数のエネルギー状態に分かれる。このエネルギー差に相当する電 磁波を当てると、共鳴現象が起きて電磁波が吸収される。その振動数は、原子核の種 類と磁場の強さで決まるが、原子核の周りの電子の状態に影響されるので、周辺の電 子の分布や原子の結合状態を知る手がかりになる。従って、NMR は分子構造の決定手 段として、また信号の強度から核スピンの数が分かるため、定量測定の手段としても 用いられる。測定対象となる物質を溶媒に溶かす溶液 NMR 法に対し、固体状態の物 質を測定する NMR 法を固体 NMR 法と呼ぶ。固体サンプルの NMR 信号は、分解能が非 常に低いが、磁場方向に対して試料を 54.7°傾けて高速回転させて計測するマジッ クアングル試料回転(MAS)法を用いることにより、分解能・感度ともに向上させる ことができる。固体サンプルの測定に広く用いられている NMR 法。NMR は Nuclear Magnetic Resonance の略。
[5] 第一原理量子化学計算
経験則や実験データに頼ることなく、量子力学理論のみを用いて電子状態を計算する 手法。最も安定なエネルギーを与える構造を計算することによって、構造の最適化を 行ったり、電子状態から NMR で観測されるパラメーターを計算できる。
[6] シメチジン、シメチジン結晶形 B
ヒスタミン H2 受容体拮抗薬として有名。胃酸の過剰分泌を抑える。合理的医薬品設 計のアプローチを用いて開発された初めての医薬品。A, B, C, D の4つの異なる結晶 形および M1, M2, M3 の水和結晶などさまざまな結晶形を取ることが知られている。 医薬品として安定した効能を発揮するためには、結晶形をコントロールすることが非 常に重要。C10H16N6S の化学式で表される。シメチジンを開発したジェームス・ワイ ト・ブラックは、1988 年にノーベル生理学医学賞を受賞。 ただし、シメチジン結晶形 B の構造は長らく未知であった。それは、結晶形 B は針 状結晶であるために、単結晶 X 線回折に必要な大きさの単結晶を作製することが困難 だったことに起因。さらに、結晶形 B は結晶形 C としばしば混ざった状態で結晶化 されることから、粉末 X 線回折による解析も困難であった。 N NH S N H N CH3 N NH CH3
[7] 賦形剤
医薬品を錠剤・散剤などの剤形において、希釈や成型のため、また取り扱いを便利に するために加えられる無害の添加物。でんぷんや糖などが広く用いられている。
[8] 透過型電子顕微鏡
通常の光学顕微鏡では可視光を試料に当てて観察するのに対し、透過型電子顕微鏡で は試料に電子線を当て、透過してきた電子線の強弱から試料の形態を観察する。電子 線の波長は可視光よりもはるかに短いため、理論上 0.1nm 程度の分解能が得られ、生 体分子やその複合体の構造解析に用いられる。ただし、電子と物質の相互作用が強いことがあだとなって、厚みのある試料を観察できない。
[9] 多孔性金属錯体(PCP/MOF)
リンカと呼ばれる多座配位子と金属イオンが配位結合することにより構成される配 位高分子。多くは多孔性を示し、ガス吸着、ガス分離、導電性など有用な物性を持 つ。PCP /MOF はPorous Coordination Polymer/Metal-Organic Frameworkの略。



