従来の200倍の回収速度を実現、実規模リチウム回収プラントの設計検討が可能に
2021-06-16 量子科学技術研究開発機構
発表のポイント
- リチウムを含む溶液から、従来の200倍の速さでリチウムを回収できる、リチウムイオン吸着性を持つイオン伝導体の開発に成功しました。
- 1.8 mg/時のリチウム回収速度の達成により生産性と経済性の飛躍的な向上が見込まれ、実規模リチウム回収プラントの設計検討が可能になりました。
- 使用済リチウムイオン電池リサイクルだけでなく塩湖かん水からのリチウム回収にも適用でき、今後予想される急激なリチウム需要の増加や日本におけるリチウムの資源循環に貢献できる技術として社会実装を進めます。
国立研究開発法人量子科学技術研究開発機構(理事長 平野俊夫。以下「量研」という。)核融合エネルギー部門六ヶ所核融合研究所増殖機能材料開発グループの星野毅上席研究員らの研究チームは、イオン伝導体を分離膜として用いたリチウム(Li)1)回収技術において、Li溶液をアルカリ性にするとともに、イオン伝導体の表面改質処理によるLiイオンの吸着性の改善によって、Li回収速度を約200倍に向上することに成功し、将来大量処理が必要な使用済Liイオン電池をリサイクルできる分離膜技術を確立しました。本技術は、Liイオン電池のLi資源循環に貢献するものであり、今後更に需要拡大が予想されるLiについて、持続可能なLi循環型社会の構築に展望を拓く大きな成果です。
蓄電池として使用されるLiイオン電池2)の材料であるLiの世界需要は、主に電気自動車(EV)市場の急拡大により、その需要が急激に伸びると予想されております。一方、2030年頃には、EV等で使用され寿命を迎える大量の使用済Liイオン電池が発生することから、Liを輸入に頼る日本では、使用済Liイオン電池のリサイクル技術の確立がLi資源循環を構築する上で不可欠です。
これまで量研では、Liだけを透過させるLiイオン伝導体3)分離膜を開発し、世界で初めて0.01mg/時のLi回収に成功していました。しかし、今後需要が高まるEV等で使用されたLi電池のリサイクルを産業として成立させるためには、電池から抽出されたLiを含む溶液の処理を更に高速化することが不可欠です。そこで、Liイオン伝導体分離膜の性能を、数mg/時とこれまでに開発した膜より100倍以上速い回収速度を持つよう改良し、大量のLi回収に適用できるようにする必要がありました。
そこで、使用済Li電池のリサイクル時に抽出される溶液と同等の700 mg/LというLi濃度の溶液を用い、Li回収速度に影響を与える要因を調べた結果、イオン伝導体表面に吸着するLiイオン数を増すことにより、回収速度を飛躍的に向上できることを見出しました。そこで、イオン伝導体表面のLiイオン吸着を阻害する水素イオンの数を減らすため、Li溶液をアルカリ性にすることによって、中性Li溶液に対してLi回収速度を140倍に向上できました。さらに、イオン伝導体表面に塩酸を用いた表面改質処理によって、Liイオン吸着促進効果を発現させることで、回収速度を当初の約200倍にまで向上でき、目標とした毎時mgオーダーである1.8mg/時の回収速度実現に成功し、Li溶液からのLi回収技術として、2021年1月5日に特許登録されました。
本技術は、使用済Li電池のリサイクルだけでなく、Li濃度が500mg/L以上の塩湖かん水4)からのLi回収にも適用可能であり、波及効果の高い技術であることから、国内でのリチウム資源循環と、海外での資源確保の両面から、カーボンニュートラル社会に向けたLiの安定確保と新産業創成に貢献できる技術として、幅広い社会実装に繋がると考えています。
本研究の一部は、科研費挑戦的萌芽研究15K14285による成果です。
研究の背景と目的
2019年ノーベル化学賞を受賞された吉野彰氏らの発明によるリチウム(Li)イオン電池は、高性能蓄電池を実現し、IT機器の高機能性化に貢献するだけでなく、電気自動車の普及促進を可能にし、環境問題の解決にも必要不可欠となっています。このLiイオン電池の正極材の原料は炭酸Li(Li2CO3)等が使用されており、その原料であるLiの世界需要は、電気自動車(EV)市場の著しい拡大に伴い、2018年で6万トン弱、2025年には20万トン程度へと急激に伸びることが予測されています。一方、供給源はチリやアルゼンチンに代表される南米など天然資源保有国に限られており、Liの安定確保は日本が克服すべき大きな課題の一つです。
南米における塩湖かん水からのLi回収では、広大な土地を利用した天日蒸発によるLi濃縮に1年以上かかるとともに、不純物元素除去などに薬剤が必要です。そのため、現在のLi資源産出国では、今後の生産拡大には生産性及び環境負荷の改善が課題とされています。これに対し、量研では核融合の燃料にLiが必要であることから、Liイオン伝導体をLi分離膜とし、簡単に超高純度Liを回収する新たな手法:LiSMIC5)を開発しておりました(図1参照)。LiSMICではLiを超高純度の水酸化リチウム水溶液として回収しますが、排CO2ガスを吹き込んで電池原料となる炭酸Li粉末を精製できるほか、回収時の副産物として水素が発生するため、これらの有効利用によって環境負荷の低い大量Li生産技術としての可能性を有しています。Liイオン電池の材料であるLiの世界需要は、主に電気自動車(EV)市場の急拡大により、その需要が急激に伸びると予想されております。同時に、寿命を迎える使用済Liイオン電池が大量に発生することから、LiSMICにて使用済Liイオン電池のリサイクルが実現すれば、日本におけるLi資源循環を構築できます。
ただし、これまでの試験条件ではイオン伝導体を透過するLiの速度、すなわちLiの回収速度が不十分であり、LiSMICの実用化には分離膜の回収速度を100倍以上にして、今までの0.01mg/時から数mg/時へのLi回収速度の向上が必要であったことから、Li回収速度向上に寄与する要因を特定する研究開発を進めてきました。
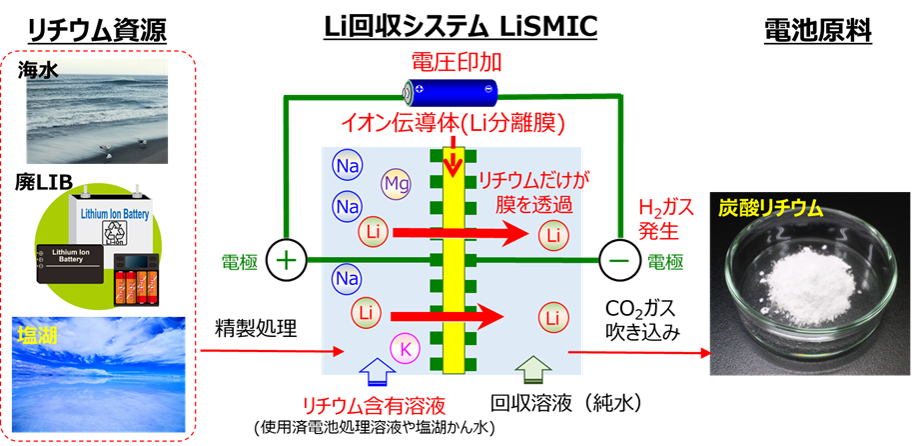
図1 LiSMICによるLi回収技術
研究内容と成果
これまでの試験では、Liイオン伝導体の一つであるLa0.57Li0.29TiO3(LLT)を分離膜として用いてきましたが、高いイオン伝導率にもかかわらず予想されるような回収速度が得られていませんでした。そこで、Li含有溶液の液性に着目し、これまで使用した中性溶液においては溶液中に多く存在する水素イオンがイオン伝導体表面に吸着し、溶液中のLiイオンが透過することを阻害していると考えました。解決策として溶液をアルカリ性にして水素イオンを減らした結果、回収速度が140倍向上することを見出しました。
また、Liイオンがイオン伝導体表面に多く存在すれば、Li回収速度の向上が期待できると考えました。そこで、量研では、LLTの表面のみを塩酸に浸漬し、Liイオン伝導体中に存在するLiを水素(H)で置換する表面改質を行うことで、LLTの表面のHと溶液中のLiイオンの交換反応を促進させる状況を作り出し、Liイオン吸着性能を発現させることに成功しました(図2)。このLi吸着性能によってLi回収速度は更に1.43倍向上し、従来のLiイオン伝導体を中性溶液にて用いた場合のLi回収速度の約200倍となる1.8mg/時にまで向上させることを達成しました(図3)。
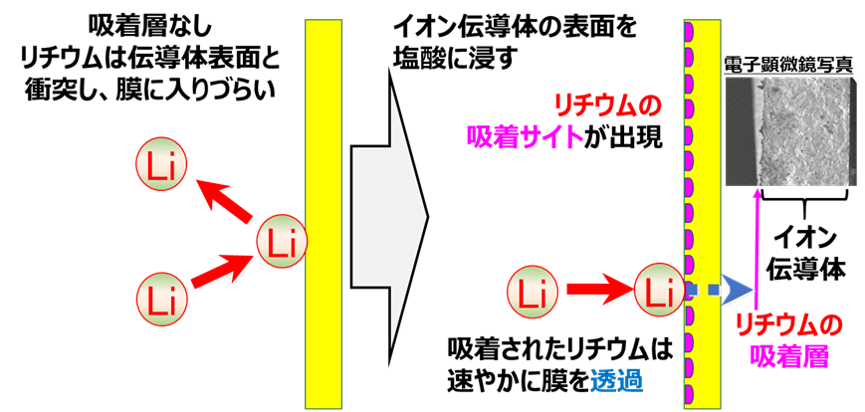
図2 Li含有容液(濃度700ppm)からのLi回収試験にて平均回収速度が約200倍向上
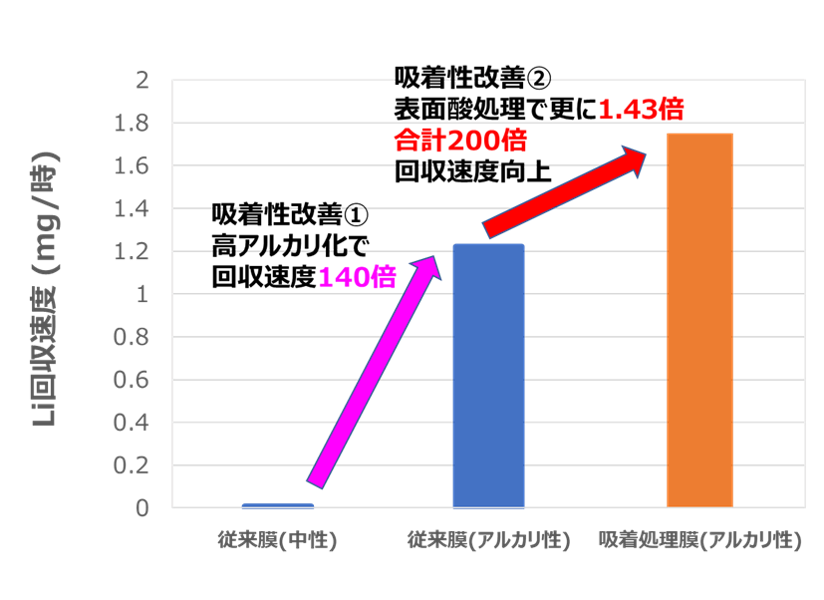
図3 Li回収量を飛躍的に向上させる表面Li吸着Liイオン伝導体
実用化に向けた取組み
量研では、この新たなLi回収技術であるLiSMICの早期社会実装を目指し、使用済Liイオン電池からのLi回収(リサイクル)の実用化を目的とした量研アライアンス6)「超高純度Li資源循環アライアンス」を設立しました。LiはEV普及促進によって地球温暖化問題を解決するためのキーマテリアルであり、低炭素社会と資源循環を同時に達成する、日本独自の自給自足な低炭素Li循環社会の実現に有用な技術です。もう一つの試みとしては、塩湖かん水からのLi回収における従来法に替わる高生産性、低環境負荷技術としてのLiSMICの適用に関する取組みも開始しました。本取組みは、国立研究開発法人科学技術振興機構の大学発新産業創出プログラム(START)事業に採択され、量研発ベンチャー設立を目標に研究開発を進めています。
研究成果の意義及び波及効果
Li含有溶液から高純度Liを高効率で直接回収することを可能とした、アルカリ性溶液への転化と新たな表面Li吸着イオン伝導体を活用し、経済性と生産性を飛躍的に向上させた使用済Liイオン電池のリサイクル技術開発に着手しました。今後、大量に発生する見込みであるEV等に使用される車載用大型Liイオン電池を工業的にリサイクルすることを可能にし、Liの安定確保(Li資源循環社会)に展望を拓く成果です。現在、独立行政法人石油天然ガス・金属鉱物資源機構、「金属資源の新製錬・回収技術の実証調査」委託研究として、「イオン伝導体分離法による使用済Liイオン電池からの高純度原料生成に関するコスト実証試験」を完遂し、早期社会実装を目指した研究活動を遂行中です。また、START事業における塩湖かん水からのLi回収の研究にも着手し、LiSMICを中軸としたLiの安定資源確保のシナリオとして、国内Li資源確保としては使用済Liイオン電池リサイクル、そして海外Li資源確保として塩湖かん水からのLi回収を行い、Li源からLiイオン電池等の製品を製造し、その製品をリサイクルする日本独自のLi資源循環社会の構築を目指します。
更に、LiSMICの副産物として発生する燃料電池に必須な水素ガス7) の利用及び排CO2ガスを利用した電池原料の一つである炭酸Li製造を通じ、省エネルギー・ゼロエミッション8)社会への貢献も期待されます。保有する特許を確実に活かしつつ、量研開発技術の早期社会実装に向けて尽力して参ります。
関連登録特許
登録特許1)LiSMICに関するもの
発明の名称:金属イオン回収装置、金属イオン回収方法
登録番号:特許第6233877号(日本)、10-2071358(韓国)、6994-B(ボリビア)
登録特許2)表面改質した新たなリチウムイオン伝導体に関するもの
発明の名称:リチウム選択透過膜、リチウム回収装置、リチウム回収方法、水素製造方法
登録番号:特許第681834(日本)、US10689766B2(米国)、10-2064692(韓国)、2017212260(オーストラリア)
用語解説
1)リチウム
リチウム(元素記号:Li)は、希少な31種類のレアメタルの中の一つです。携帯電話、ノートパソコン等の充電用電池である小型リチウムイオン電池、電気自動車、家庭用蓄電池用の大型リチウムイオン電池の原料です。リチウム資源は、地上埋蔵量(南米、オーストラリア等に偏在)は約1600万トン、海水中に含まれる量は2,300億万トンと推定されています。
2) リチウムイオン電池
リチウムイオンによって充電や放電を行う二次電池です。電極には、リチウムイオンを可逆的に出し入れできる材料が使われ、正極の代表的な材料にはニッケル酸リチウム、コバルト酸リチウム、マンガン酸リチウムの3種類があります。負極の材料としては炭素系素材やチタン酸リチウムが使われます。電極間でのリチウムイオンのやり取りを担うため、電池内部は有機材料の電解質で満たされています。
3) イオン伝導体
融点よりかなり低い温度においてある特定のイオン(伝導イオン)が拡散する 固体物質のことで、主にセラミックスや高分子シート等の、イオンを伝導させる性質を有する材料です。本研究ではペロブスカイト型リチウムイオン伝導性酸化物の1つであるLa2/3-x Li3xTiO3(LLT)を用いました。他のイオン伝導体としては、NASICON型結晶構造のセラミックスのイオン伝導体等、様々なイオン伝導体が存在します。
4) 塩湖かん水
塩湖とは、水1L中に 0.5g以上の塩類を含む湖を指し、かん水とはその水のこと。リチウム産出の塩湖では、チリのアタカマ湖、アルゼンチンのオラロス塩湖、ボリビアのウユニ湖が有名。
5) LiSMIC
イオン伝導体リチウム分離法(Li Separation Method by Ionic Conductor)を表します。リチウムを含む原液とリチウムを含まない回収溶液間をイオン伝導体の分離膜で隔離し、原液と回収溶液間に電圧を印加することで、原液に含まれるリチウムを回収溶液へ選択的に移動させて濃縮回収する量研独自の方法です。使用済みリチウムイオン電池の処理溶液のほかに、海水、塩湖かん水、にがりなどからリチウムを回収する革新的な方法として期待されています。
6) 量研アライアンス
産業界に存在する技術的課題を解決し、そのブレークスルーによって当該業界にイノベーションを創出するため、量研と特定分野の企業群が共同で研究開発を行うアライアンス事業を行っております。その事業の一つとして、2018年12月に超高純度リチウム資源循環アライアンスを設立し、高品位なリチウムイオン電池用原材料を使用済リチウムイオン電池から再資源化する、リチウム資源循環技術の社会実装を目指した研究開発を行っています。
7) 水素ガス
イオン伝導体中をイオンが移動することで、イオン伝導体の両端に設置した電極間を電子が流れます。回収溶液側(-極)では、水素イオンがこの電子を受け取り、水素ガスになる反応が生じます。
8) ゼロ・エミッション
資源回収やリサイクルでは、必要とする資源が得られると同時に、化石燃料や電気等の外部エネルギーを消費するため、地球環境への負荷もかかります。本技術では、リチウム回収副産物である水素ガスを貯蔵し、燃料電池などへ水素エネルギーを有効利用することで、地球環境への負荷をゼロにするゼロ・エミッションを目指すことが可能になります。