2019-09-30 量子科学技術研究開発機構
ポイント
- 単色X線※1)と多孔性シリカナノ粒子※2)を用いることで、がんの患部でX線のエネルギー効果を増幅できる方法を開発することに成功
- ナノ粒子によりがん細胞の細胞核近傍へガドリニウムを届けることが可能に
- 50.25 keVの単色X線により、卵巣がんの塊をばらばらにし、がん細胞を消滅させることに成功

京都大学アイセムスの玉野井冬彦(たまのい・ふゆひこ)特定教授、松本光太郎(まつもと・こうたろう)特定助教、量子科学技術研究開発機構 関西光科学研究所の齋藤寛之(さいとう・ひろゆき)上席研究員らのグループは、単一エネルギーをもつX線すなわち単色X線を、ガドリニウムを多孔性シリカナノ粒子により取り込ませたがんの塊に照射することで、その塊がばらばらになり消滅することを明らかにしました。
現在、放射線治療はがん治療の主要な方法として広く使われていますが、既存のX線は、幅広い波長が含まれているため、皮膚表面でX線が吸収されてしまい、がん組織に届きにくいという課題がありました。研究グループは、1925年にピエール・オージェらが報告した原理を利用し、単色X線を、がん細胞に取り込ませたガドリニウムに照射することでオージェ電子が放出される原理を使い、がん細胞を死滅させることを目指しました。
ガドリニウムは、研究グループが独自に開発した多孔性シリカナノ粒子を用いてがん細胞の中に送り込み、単色X線は、大型放射光施設(SPring-8)の量研専用ビームラインBL14B1において照射しました。結果、卵巣がんの塊に対して、ガドリニウムからオージェ電子を放出させるのに最も適した50.25 keVのX線を照射した場合に、効果的にがん細胞を攻撃できることが明らかになりました。多孔性シリカナノ粒子の働きにより、ガドリニウムをがん細胞の細胞核近傍に局在させたことが、成功の鍵となりました。ピエール・オージェらの発表から100年の時を経て、新たな治療法開発における一歩になります。
本成果は英国時間9月30日午前10時(日本時間 午後6時)に、英科学誌「Scientific Reports(サイエンティフィック・リポーツ)」オンライン版で公開予定です。
1. 背景
現在、放射線治療はがん治療の主要な治療として広く使われています。しかしながら、既存の放射線治療には、放射線の大部分が皮膚表面に吸収されてしまい、患部に届く放射線が少ないという課題があります。また、通常、放射線治療に用いられるX線は様々な元素と相互作用を起こし、正常細胞へも影響を及ぼしてしまいます。例えば、皮膚表面でX線が吸収されることで、皮膚の炎症など副作用が起きてしまいます。そこで、がん以外の正常な細胞に影響を与えない単一エネルギーをもったX線すなわち単色X線による選択的吸収方法の開発が期待されていました。そこで、私達は、様々な単色X線を作り出すことができる大型放射光施設SPring-8(兵庫県佐用郡)の放射光ビームラインを利用して、単色X線をがん治療に応用する研究をはじめました。
単色X線を用いるというアイディアは、1923年にピエール・オージェらが示した重要な発見を基にしています。この発見では、金やガドリニウムなどの高Z元素※3)にX線を照射すると電子が軌道からたたき出されるということが示されました(オージェ効果※4))。放出された電子はDNAへの損傷効果が高く、細胞を殺すことができます。この原理を用いてがん治療を開発する試みは行われてきましたが、金やガドリニウムなどの高Z元素を効果的にがん細胞の中へ送り込む仕組みが確立できず、なかなか突破口が得られていませんでした。また、本研究においては、オージェ効果が最も強く起こる吸収端※5)近傍のX線のエネルギーを制御することが極めて重要となりますが、実験室系の装置ではその制御が困難であったこともその要因の一つと言えます。
2. 研究内容と成果
私達は今回、卵巣がんのスフェロイド※6)の内部にガドリニウムを取り込ませ、SPring-8の量研専用ビームラインBL14B1において、ガドリニウムのK殻吸収端である50.25KeVのエネルギーをもつ単色X線を照射することで、がんの塊をバラバラにしてさらに消滅させることに成功しました。図1の通り、照射時間10分でがん細胞が大幅に減少し、60分照射においては、がん細胞が完全に消滅していることが分かります。この実験により、単色X線とガドリニウムを取り込ませた多孔性ナノ粒子の組み合わせが、新規の放射線治療に有効であることを明らかにしました。将来、他のがん、脳腫瘍、肺がんなどにも応用を広げることができると思われます。
成功の鍵は多孔性シリカナノ粒子を使ったことにあります。私達は、これまでにアイセムスで多孔性シリカナノ粒子を開発し、がん治療への応用を目指してきました。すでに多孔性シリカナノ粒子のがん細胞への取り込み、がんへの蓄積に関して良い知見を示しています。今回、この多孔性シリカナノ粒子にガドリニウムを含有させ、がんの塊であるスフェロイドの深部にまでガドリニウムを送り込むことに成功しました。ナノ粒子の分布を調べたところ、がん細胞の中に取り込まれ、DNAのある細胞核の近傍に位置することが明らかになりました。つまり、ガドリニウムをDNAの近くに高濃度で局在させることができたということです。
ガドリニウムを含有していない多孔性シリカナノ粒子を用いた場合には、単色X線照射の影響はみられませんでしたので、使用した単色X線は正常細胞に対して、大きな影響はないと考えられます。
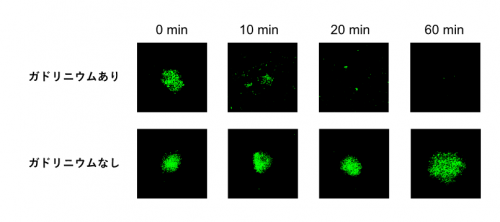
図1 単色X線の照射時間とがん細胞のかたまり(がんスフェロイド)へ与える影響
ガドリニウムの取り込んだがんスフェロイドは、単色X線の照射により、ばらばらになり死滅する。 緑(GFP):生細胞
驚くべきことに、この照射実験の結果においては、ガドリニウムのK殻吸収端近傍のエネルギーである50.25 keVのX線で見られるがんの消滅効果が、吸収端より僅かに低い50.0 keVでは見られませんでした(図2参照)。この結果は、このがんの死滅がオージェ効果に起因することを示唆していると考えられます。
このように正確にエネルギー制御された単色X線とガドリニウム含有多孔性シリカナノ粒子の組み合わせが、がん死滅に対して劇的な効果を生むことを実証することができました。こうした単色X線と適切な元素選択の組み合わせにより、新たな放射線治療の可能性が拓かれることが期待できます。
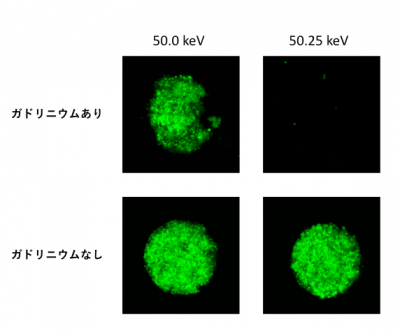
図2 単色X線のエネルギーの差ががんスフェロイドに与える影響
がんスフェロイドにガドリニウムを取り込ませ、単色X線を当てたときの影響を調べたところ、50.0 keVではがんスフェロイドに影響を与えず(左上)、50.25 keVの場合には、効率的にがんスフェロイドを死滅させることができる(右上)。緑(GFP):生細胞
3. 今後の展開
私達の開発したナノ粒子は高いがんへの蓄積能を示しています。また、以前からの研究で、がんを移植したマウスなどにナノ粒子を静脈注射するとがんに選択的に蓄積することを、明らかにしています。今後の展開の一つとして動物実験を予定しています。
今回は卵巣がんの細胞から作ったがんスフェロイドをもちいましたが、治療の対象としてはさまざまな種類のがんへの応用が期待されます。たとえば食道がんの場合、内視鏡でがんを検出して、そこにガドリニウムを含有したナノ粒子を打ち込み、そして単色X線の照射を行うという手順をとることが考えられます。
高Z元素として、ガドリニウムを使いましたが別の元素を使うこともできます。ヨウ素を使うとより低いエネルギーの単色X線を用いることができるため、現在検討中です。
4. 用語解説
※1 単色X線:単一エネルギーを持つX線。モノクロメーターを用いてX線から取り出す。
※2 多孔性シリカナノ粒子:シリカ骨格をもつ約100nm直径のナノ粒子。多孔性である特徴がある。
※3 高Z元素:原子番号の大きい元素
※4 オージェ効果:外部からのX線や粒子線の照射により元素の内殻に空孔が生じたとき,この空孔へ外殻にある電子が遷移してくる。外殻の他の電子がそのときに放出されるエネルギーを受け取り放出される。
※5 吸収端:原子の内殻(K,L殻)電子の励起に伴う吸収が起こり始める、元素に固有のエネルギーのこと。吸収端においては、X線の吸収が急激に大きくなる。
※6 スフェロイド: がん細胞が3次元的に増殖することにより得られるがんのかたまり。
5. 研究プロジェクトについて
本研究は、独立行政法人 日本学術振興会科学研究費補助金により行われています。
6. 論文タイトル・著者
“Destruction of tumor mass by gadolinium-loaded nanoparticles irradiated with monochromatic X-rays: Implications for the Auger therapy”
(ガドリニウム含有ナノ粒子と単色X線の照射によるがんの塊の消滅:オージェ治療の可能性)
著者:Kotaro Matsumoto, Hiroyuki Saitoh, Tan Le Hoang Doan, Ayumi Shiro, Keigo Nakai, Aoi Komatsu, Masahiko Tsujimoto, Ryo Yasuda, Tetsuya Kawachi, Toshiki Tajima, Fuyuhiko Tamanoi
Scientific Reports|DOI: 10.1038/s41598-019-49978-1