2019-1-14 東京大学
本研究成果は2019年1月14日付でNature Communications (オンライン版)に掲載されました。
発表概要
天然由来のアルカロイドはヘテロ原子同士の結合を含むものが数多く存在し、それらの生合成からは新規骨格形成酵素の発掘が期待されます。sulfoneamide、6-azatetrahydroindane骨格を含むaltemicidin、SB-203208化合物は抗腫瘍活性、抗微生物活性を持つ細菌由来抗生物質として知られていました。本研究グループは、これらの化合物の生合成酵素遺伝子を見出し、これらの中の一つの酸化酵素によって、L-cysteineから二段階の酸化を経て、S-N結合を含む2-sulfamoylacetic acid形成までが触媒されることを示しました。一段階目の脱炭酸と連携した一酸素原子添加反応は硫黄原子の反応性を活かした、前例のない新規性の高い反応でした。今後、本研究の結果を元に、天然のS-N結合化合物の骨格形成反応の解明と多段化酸化酵素を用いた物質生産への応用研究が発展し、創薬研究に大きく貢献することが期待されます。
本研究成果は、安価で豊富な炭素資源を価値の高い分子へと効率的にアップグレードする化学プロセスへの応用が期待されます。
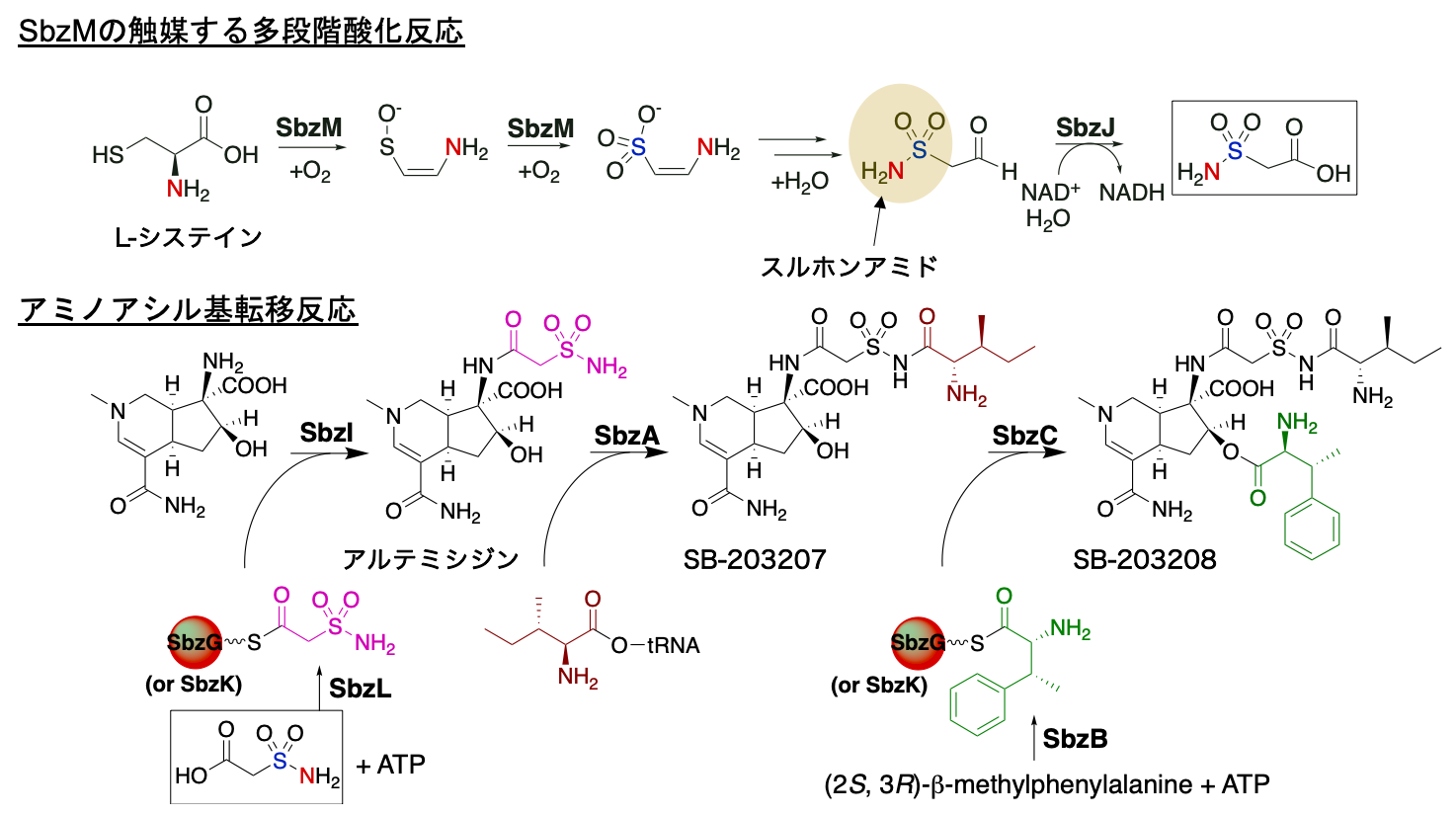
図:本研究において明らかとなった新規スルホンアミド天然物骨格形成反応
論文情報
Zhijuan Hu*, Takayoshi Awakawa*, Zhongjun Ma, Ikuro Abe (* co-first author), “Aminoacyl sulfonamide assembly in SB-203208 biosynthesis,” Nature Communications: 2019年1月14日, doi:10.1038/s41467-018-08093-x.
論文へのリンク (掲載誌)
関連教員
淡川 孝義 / 講師 / 大学院薬学系研究科
阿部 郁朗 / 教授 / 大学院薬学系研究
スルホンアミド骨格を形成する新規酸化酵素の発見
〜多段階酸化酵素によるアミノ酸由来天然物の新奇骨格形成〜
1. 発表者:
胡 志娟(東京大学大学院 薬学系研究科 博士課程3年生)
淡川 孝義(東京大学大学院 薬学系研究科 講師)
阿部 郁朗(東京大学大学院 薬学系研究科 教授)
2.発表のポイント:
◆天然由来アルカロイドであるスルホンアミド抗生物質生合成に関わる新規酸化酵素を発見 した。
◆アミノ酸を基質として受け入れ S-N 結合形成までを導く前例のない多段階酸化反応を触媒 する酵素の同定に成功した。
◆S-N 結合含有天然物の骨格形成反応の解明と多段化酸化酵素を用いた物質生産への応用を 通して、創薬研究の発展に貢献することが期待される。
3.発表概要:
天然由来アルカロイドはヘテロ原子同士の結合を含むものが数多く存在し、それらの生合成 からは新規な骨格形成酵素の発掘が期待されます。スルホンアミド、特異な二環性骨格を含む アルテミシジン、SB-203208 化合物は抗腫瘍活性、抗微生物活性を持つ細菌由来抗生物質と して知られていました。東京大学大学院薬学系研究科の胡志娟大学院生、淡川孝義講師、阿部 郁朗教授の研究グループは、これらの化合物を生産する放線菌より生合成酵素を同定し、その うちの一つの酸化酵素によって、L-システインから二段階の酸化を経て、S-N 結合形成まで が触媒され、スルホンアミド構造が生成する新規な生合成酵素反応を示すことに成功しました。
一段階目の脱炭酸と連携した一酸素原子添加反応は硫黄原子の反応性を活かした前例のない 反応でした。今後、本研究の結果を元に、天然の S-N 結合化合物の骨格形成反応の解明と多 段化酸化酵素を用いた物質生産への応用研究が発展し、創薬研究に大きく貢献することが期待 されます。
4.発表内容:
天然物は現在も医薬品資源として重要な役割を果たしています。しかし、古典的な手法によ る新規化合物単離数は減少の一途をたどり、新たな物質生産の手法が求められています。その 中でも、生合成酵素を用いた新規物質生産手法が注目を集めています。そのためには、新たな 化合物を合成する酵素を発掘し、その詳細な機能解析をすることが重要となります。天然由来 のアルカロイド(注1)はヘテロ原子(注2)同士の結合を含むものが数多く存在し、それら の生合成からは新規な骨格形成酵素の発掘が期待されます。時に化学合成困難な骨格も存在し、 これら化合物の酵素合成には興味が持たれます。しかしながら、これら生合成酵素のうち同定 されているものは僅かであり、物質生産へと応用するためには、多くの酵素を同定し、その反 応解析を行い、より詳細な酵素反応の知見を得る必要があります。 海洋から単離される放線菌(注3)Streptomyces sp.株が生産するアルカロイド化合物であ る、アルテミシジン、SB-203208 は抗腫瘍活性、抗微生物活性などさまざまな活性を示す、 創薬シードとして有望な研究対象の一つです。これら化合物は、スルホンアミド(注4)、特 異な二環性骨格を含み、その骨格の複雑さから全合成研究のターゲットとなってきました(図)。 スルホンアミドは弱塩基性を示し、より剛直な骨格を形成する官能基であり、その生合成に関 わる酵素の発掘は注目を集めていました。しかし、過去に前例のない新規骨格の生合成である ために、相同性ベースでの生合成遺伝子探索の手法を適用することが難しいという問題があり ました。
今回、研究グループは、SB-203208 がアミノアシル tRNA 合成酵素(注5)阻害活性を持 つことを手掛かりに、その生合成酵素遺伝子クラスターを見出しました。その中から、tRNA 依存型アミノアシル基転移酵素 SbzA などいくつかのアミノ酸側鎖修飾に関わる新規酵素を 同定しました(図)。また、スルホンアミド構造の生合成に関わる二種の酸化酵素 SbzJ, SbzM を同定し、金属酵素(注6)である SbzM がシステインから二段階の酸化を経て S-N 結合形 成までの反応を導き、スルホンアミド形成を行う新規性の高い金属酸化酵素であることを示し ました(図)。一段階目の反応では、SbzM はヒスチジンに配位された鉄原子が酸素原子を活 性化し、活性化された酸素がシステインの硫黄原子と反応し、いくつかの反応ステップを経て 不安定なスルフィン(注7)中間体を与えます。この不安定構造が脱炭酸と脱炭酸と連携して、 一酸素原子添加されるのですが、この反応は前例がなく、硫黄原子の反応性を活かした興味深 い反応でした。SbzM は単独でアミノ酸からスルホンアミドを形成する、非常に新規性の高い 酸化酵素であり、インパクトの大きな研究結果となりました。 本研究では、特異な骨格を持つ微生物二次代謝産物に注目し、その生合成経路を探索するこ とで、S-N 結合形成に関わる新規酸化酵素を同定し、医薬品シードとしての可能性を秘める スルホンアミドアルカロイド化合物群の生合成に関する知見を取得しました。多段階の酸化反 応は興味深く、本研究成果を元に、立体構造解析、反応中間体エネルギー計算など、金属酸化 酵素の反応機構や制御に関わる研究が進展することが期待されます。得られた知見によって、 医薬品活性を持つアルカロイド類縁体を、酵素法によって簡便に生産する系が構築され、創薬 研究に大きく貢献することが期待されます。 本研究は、文部科学省 科学研究費補助金、新学術領域研究(研究領域提案型)「生物合成 系の再設計による複雑骨格機能分子の革新的創成科学(生合成リデザイン)」の支援を受けて 行われました。
5.発表雑誌:
雑誌名:Nature Communications
論文タイトル:Aminoacyl sulfonamide assembly in SB-203208 biosynthesis
著者:Zhijuan Hu*, Takayoshi Awakawa*, Zhongjun Ma, Ikuro Abe (* co-first author) DOI 番号:10.1038/s41467-018-08093-x
アブストラクト URL:http://www.nature.com/ncomms.
6.問い合わせ先:
【研究に関するお問い合わせ】
東京大学大学院 薬学系研究科 薬科学専攻 教授 阿部 郁朗(あべ いくろう)
【報道に関するお問い合わせ】
東京大学大学院 薬学系研究科 庶務チーム
7.用語解説:
(注1)アルカロイド:窒素原子を含む天然由来有機化合物の総称。薬理作用を持つものが多 く含まれる。
(注2)ヘテロ原子:炭素、水素以外の原子のこと
(注3)放線菌:土壌などさまざまな環境に存在し、数々の医薬品シード化合物を合成する細 菌の一種。
(注4)スルホンアミド:R1−SO2−NR2R3 構造を持つ化合物群。 カルボン酸のアミドに比 べ、酸や塩基による加水分解、ヒドリド還元などに対して一般に安定である。
(注5)アミノアシル tRNA 合成酵素:特定のアミノ酸に対応する tRNA にエステル結合さ せてアミノアシル tRNA を合成する酵素。
(注6)金属酵素:補因子として金属を含む酵素。金属はタンパク質の側鎖、あるいはタンパ ク質以外のポルフィリンなどの有機化合物に配位して存在する。金属と酸素間の電子のやりと りにより、酸素原子が活性化され、多様な酸化、還元反応が触媒される。
(注7)スルフィン:C=S=O の構造を持ち、その不安定性から反応性に富む。
8.添付資料:
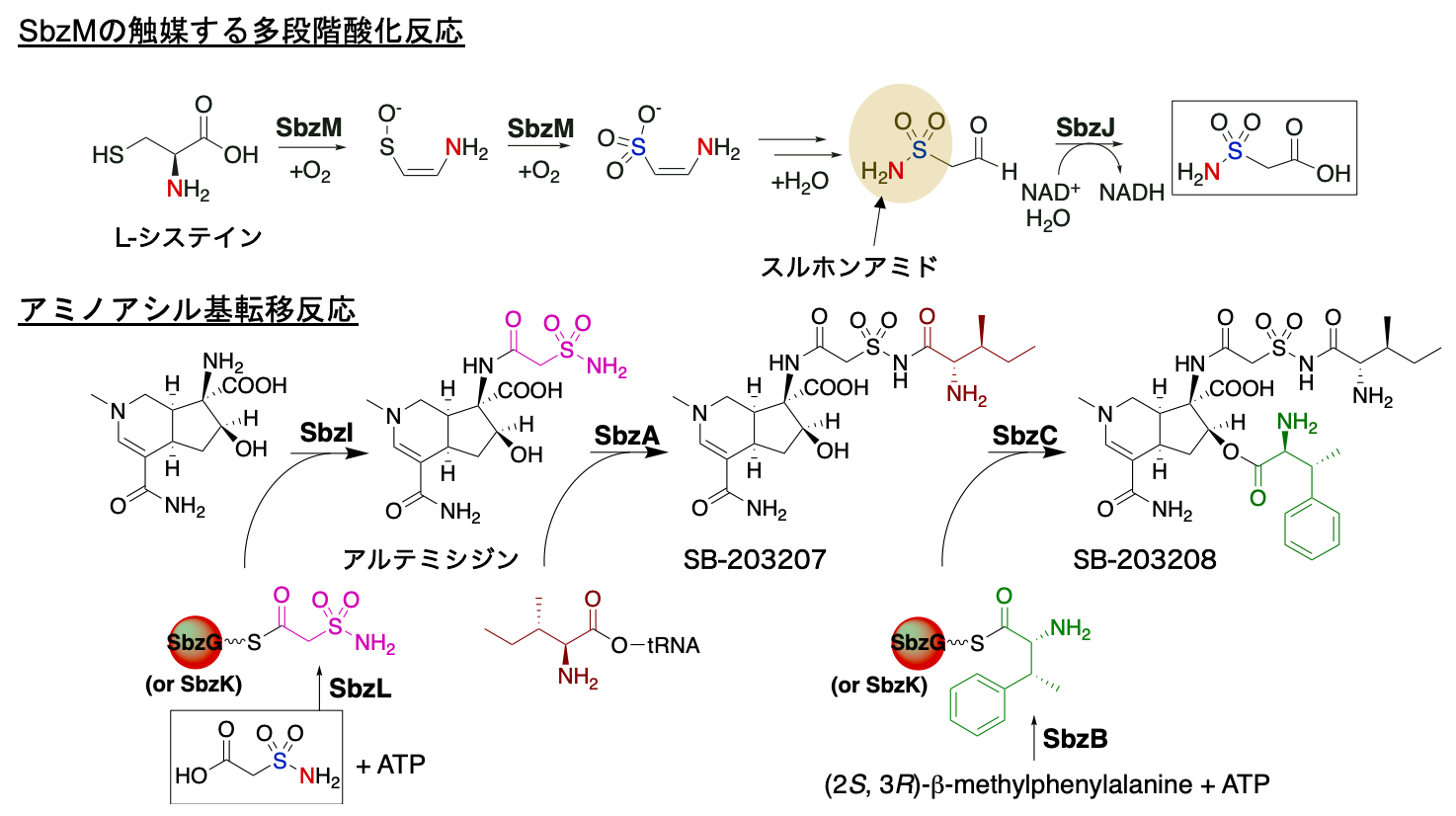
図:本研究において明らかとなった新規スルホンアミド天然物骨格形成反応