2018/11/28 量子科学技術研究開発機構
発表のポイント
- 放射線に強い細菌の鍵となるタンパク質の立体構造を世界で初めて決定
- 鍵となるタンパク質がDNAの傷を治す機能を解析し、これまでに例のないタンパク質とDNAとの複合体構造を示唆
- DNAの傷を効率よく修復するメカニズムの解明が飛躍的に進み、放射線障害やがん化抑制の医療への貢献に期待
国立研究開発法人 量子科学技術研究開発機構(理事長 平野俊夫、以下「量研」という)量子ビーム科学研究部門高崎量子応用研究所の安達基泰プロジェクトリーダーらのグループは、放射線に強い細菌の中に含まれ、その強さの鍵となるタンパク質について、分子の立体構造とその機能発揮に重要な役割を果たすアミノ酸を世界で初めて明らかにしました。放射線で傷ついた遺伝子を修復するタンパク質を原子レベルで正確に捉えたものであり、放射線障害やがん化抑制の医療への貢献が期待されます。
ヒトよりも1,000倍以上放射線に強い性質を持つ“放射線抵抗性”細菌、デイノコッカス・ラディオデュランスは、放射線照射により生じるDNAの“傷”である二本鎖切断を効率よく修復する能力を持っています。しかしながら、この放射線に対する「強さ」を獲得した細菌が、放射線から身を守り、DNAを修復する優れた能力を発揮するためのメカニズムについては、未だ多くの謎が残されています。これまでの研究から、この細菌にはPprAと呼ばれるその細菌の仲間しか持っていないユニークな“DNAに結びつくタンパク質”が存在することが知られています。このため、「強さ」の謎を解くには、まずPprAの立体構造を知ることが必要でした。
今回、茨城県つくば市の高エネルギー加速器研究機構放射光科学研究施設(KEK-PF)と、兵庫県佐用町の高輝度光科学研究センター大型放射光施設(SPring-8)のX線を用いてPprAの立体構造を解析し、8個のPprAが連なり、約40nmで一つのユニットを形成する長く特徴的な“らせん構造”をもつことを見出しました。さらに、PprAとDNAとの結合の様子を分析し、DNAの“傷”を修復する機能を発揮するために必要な4つのアミノ酸を特定するとともに、一般的なタンパク質には類のない構造でDNAを引き伸ばすことを示しました。本成果を基に、放射線により生じたDNAの傷を効率よく修復するメカニズムの解明が飛躍的に進み、将来、放射線障害やがん化の抑制につながることが期待されます。
この研究の一部は、文部科学省科学研究費補助金において実施した成果です。なお、本研究成果は、2018年11月下旬頃(予定)に 「Federation of American Societies for Experimental Biology(FASEB)」の発行するThe FASEB Journal誌のオンライン版に掲載されます。
背景
生物が強い放射線を受けたとき、生きていくために必要なDNAやタンパク質などの分子が壊されます。DNAについては、次の世代をつくるための遺伝情報をもった生命の活動に欠かせない唯一の分子です。そして、生物(細胞)は、DNAの放射線による損傷を修復する一連のタンパク質を持ち、これらのタンパク質によりDNAを修復することができます。生物が強い放射線の照射を受けると、損傷を十分に修復できず、障害が残ることがありますが、放射線に対する感受性は生物の種によって大きく異なります。その中で、放射線抵抗性細菌と呼ばれるデイノコッカス・ラディオデュランス(図1)は、ヒトよりも1,000倍以上放射線に強い性質をもっていることが知られています。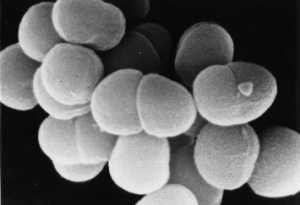 このため、数千グレイ1)という、ヒトにとっては致死量をはるかに超えた量の放射線を浴びても、生き残ることができます。この「強さ」は、放射線照射により生じるDNAの二本鎖切断2)を効率よく修復する能力によって得られたものと考えられています。それは、生命が地球上で進化してきた中で獲得した優れた能力の一つであり、生命の神秘の一つです。しかしながら、その細菌が放射線から身を守る優れた能力を発揮する分子メカニズムについては、未だ多くの謎が残されているのが現状です。
このため、数千グレイ1)という、ヒトにとっては致死量をはるかに超えた量の放射線を浴びても、生き残ることができます。この「強さ」は、放射線照射により生じるDNAの二本鎖切断2)を効率よく修復する能力によって得られたものと考えられています。それは、生命が地球上で進化してきた中で獲得した優れた能力の一つであり、生命の神秘の一つです。しかしながら、その細菌が放射線から身を守る優れた能力を発揮する分子メカニズムについては、未だ多くの謎が残されているのが現状です。
研究の課題
放射線に強いデイノコッカス・ラディオデュランスは、今から約60年前の1956年に、アメリカで見つかった細菌です。牛肉の缶詰にガンマ線を照射して滅菌しても、生き残る細菌があるということが発見のきっかけでした。その後、20世紀の終わりには、デイノコッカス・ラディオデュランスを放射性廃棄物の処理に利用するため、米国ゲノム研究所がゲノム配列(全DNA配列)を決定しました(ヒトのゲノム配列の決定よりも数年早い)。ゲノム配列の決定は、細菌が持つDNAの損傷を修復する一連のタンパク質を決めるための基礎情報として不可欠なものですが、実際にどのようなメカニズムで、損傷されたDNAが効率よく修復されるのかは、明らかとなっていませんでした。このため、DNAの修復に関わる分子一つ一つがどのような機能をもって、それらがどのように協力し合っているのかを調べることが課題となります。
研究の概要
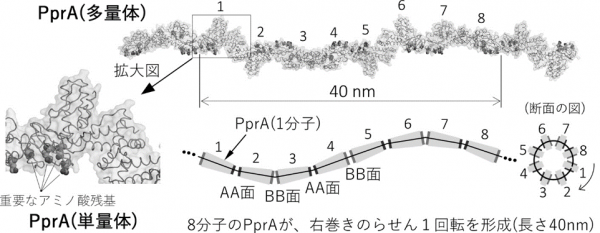
当研究グループは、デイノコッカス・ラディオデュランスのもつPprA3)と呼ばれるデイノコッカス属の細菌しかもたない特有のタンパク質に着目しました。他の生物が持たない優れた能力の謎を解くためには、その細菌にしかないタンパク質分子が、鍵を握っているものと考えられるからです。今回、そのPprAの原子レベルの立体構造を世界で初めて明らかにするとともに、PprAとの機能発現に重要な働きをする部位を見出すことができました(図2)。放射線に強い細菌の謎を解くにあたって、研究の飛躍的進展につながる成果です。
図2
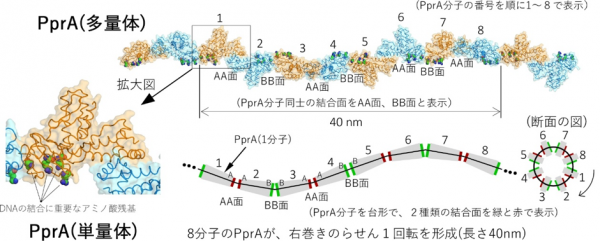
研究の内容
本研究で着目するPprAは、分子量が3万の分子であり、タンパク質としては比較的小さな分子です。これまでの研究で、① PprAが細菌の中に存在しないと放射線に対して非常に弱くなること [PprAが放射線抵抗性に重要な役割を果たしていること]、② PprAは2本鎖DNAに結合する(結びつく)能力があること [PprAはDNA修復を担うタンパク質であること]、③ PprAはいくつかの分子が結合した多量体構造をもつこと [ただし詳細な構造は不明]が、明らかになっていました。PprAが、どのような機能をもってDNAを修復しているのかを明らかにしていくためには、まず、原子レベルでPprAの立体構造を知る必要がありました。そこで、研究グループは、立体構造を明らかにするためX線結晶構造解析4)を行いました。
実験の概要
X線結晶構造解析を行うことで、原子レベルで立体構造を決定することができますが、そのためには質の高い結晶の作製が必要です。しかしながら、PprAそのものは多量体構造をもつことから、質の高い結晶の作製が困難でした。そこでグループでは、PprAの2種類の変異型5)(A139RとW183R)を作製し、多量体構造を2量体構造に変換することで、質の高い結晶の作製に成功し、X線結晶構造解析を完成しました(図2)。X線結晶構造解析のデータ収集には、茨城県つくば市の高エネルギー加速器研究機構放射光科学研究施設KEK-PFと、兵庫県佐用町の高輝度光科学研究センター大型放射光施設(SPring-8)の良質なX線を用いました。また、SPring-8のX線を用いて小角散乱6)データを収集し、PprAが溶液中で繊維状の構造をもつことを明らかにしました。最終的に、得られたデータをコンピューターグラフィックスと科学計算で解析することによって、PprAの構造を原子レベルで決定し、PprAのもつ多量体構造の詳細を決定しました。さらに、PprAがDNAの結合に重要な部位を調べるために、変異を導入したPprAを複数作製し、PprAとDNAとの結合の様子を分析した実験によって、PprAの表面に位置しDNAの結合に必ず必要となる4つのアミノ酸(Lys[リシン]133, Arg[アルギニン]150, Arg252, Lys256)を同定しました。
成果のポイント
今回解析したPprAは、デイノコッカス属のみがもつ特有のタンパク質です。X線結晶構造解析によって分子の構造を原子レベルで明らかにするとともに、機能解析実験によりPprAの中でDNAの結合に重要な部位を調べることで、次のような詳しい情報が明らかになりました。
1) PprAが集まって繊維状の多量体を形成し、分子が互い違いに逆を向く、これまでに報告例のない新しい構造をもっていること。
2) PprAの多量体は、8分子が一つの単位としてらせん構造を有しており、その一つの単位の長さは、40nmとタンパク質としては極めて長いこと。
3) PprAは、同じくDNAの修復に関わるRecA7)タンパク質やDNAと同じ右巻きのらせん構造をもっていること。
4) PprAのらせん構造の中心にDNAの結合に重要な4つのアミノ酸があること。
以上の結果と、過去の実験結果とを合わせて推測すると、PprAが、DNAを1.5倍の長さに引き伸ばしているものと考えられます(図3)。このことは、DNA修復メカニズム解明において、PprAがこれまでにない新しい機能をもっていることを示す非常に重要な知見です。例えば、細胞がDNAを修復する際において、PprAがDNAの一部を交換する反応を促進していることが考えられます。
図3
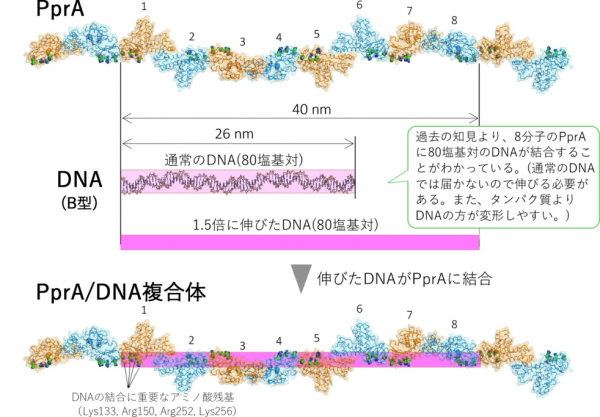
今後の展開
今後は、今回得られた情報をもとに、実際にDNAの構造がどのように変形しているかを明らかにし、さらにPprA以外のどのようなタンパク質と、どのように協力してDNAを修復するかという分子のメカニズムを解明していきます。PprAが、これまでにない全く新しい構造をもつことがわかりましたが、そのことは、PprAがこれまでに見つかっていないメカニズムで、効率よくDNAを修復していることを示しています。
成果の波及効果
本研究で得られた成果によって、DNAの二本鎖切断を効率よく修復する能力の中で、分子一つ一つがどのような機能をもって、それらがどのように協力し合っているかを研究するための土台ができました。今後放射線に強い細菌の謎を解く研究が、飛躍的に進展すると考えられます。DNAの二本鎖切断の修復は、放射線に強い細菌だけにみられることではなく、放射線を受けたときの障害の原因や、ヒトのがん細胞の形成との関わりが深いために、放射線防護の観点や、がんの予防や治療に役立つ知見の取得につながるものです。現在、研究グループは、PprAをはじめとして、DNAの二本鎖切断の修復に関わるタンパク質の機能解析研究をすすめており、”放射線に強い細菌の謎の解明”に向けた研究に引き続き取り組んでいます。
共同研究者など
本研究は、量子科学技術研究開発機構量子ビーム科学研究部門高崎量子応用研究所の安達 基泰プロジェクトリーダーが中心になって実施しました。共同研究者は、同研究所の清水 瑠美 主任技術員、柴崎 千枝 業務補助員、佐藤 勝也 上席研究員、藤原 悟 上席研究員、新井 栄揮 上席研究員の5名の他、黒木 良太 博士(故人)、鳴海 一成 博士(現 東洋大学 教授)です。また、本研究の一部は、文部科学省科学研究費補助金(計3件)によって行いました。
論文について
「Extended Structure of Pleiotropic DNA Repair-Promoting Protein PprA from Deinococcus radiodurans」
執筆者・所属
Motoyasu Adachi1, Rumi Shimizu1, Chie Shibazaki1, Katsuya Satoh1, Satoru Fujiwara1, Shigeki Arai1, Issay Narumi2, and Ryota Kuroki2
1国立研究開発法人量子科学技術研究開発機構 量子ビーム科学研究部門
2国立研究開発法人日本原子力研究開発機構
用語説明
1) グレイ
電離放射線が生物や物質に与えたエネルギーを表す単位であり、物質 1kgにつき1Jのエネルギーが与えられるときの吸収線量を1グレイ(Glay)として定義されている。
2) 二本鎖切断
DNAは、A,T,G,Cの4つの塩基が重合した2つの鎖が、らせん状に巻いた構造をもっている。その2つの両方の鎖が切断されること。
3) PprA
Pleiotropic protein promoting DNA repair A を略してPprA。デイノコッカス・ラディオデュランスのPprAは、284個のアミノ酸からなる比較的小さなタンパク質で、デイノコッカス属しかもたないユニークなタンパク質である。
4) 結晶構造解析
規則正しく分子が並んだ結晶試料を作製し、試料にX線や中性子などの量子ビームを照射すると回折現象が起こる。回折した量子ビームを観測し、得られたデータをフーリエ変換することで、試料(分子の)の原子座標が得られる分析方法。
5) 変異
DNAであれば、A,T,G,Cの4つの塩基が別の塩基に置換されていることで、タンパク質であれば別のアミノ酸に置換されていること。タンパク質は、DNAの配列情報をもとに合成されるため、タンパク質を人工で合成するために使っているDNAに変異を入れることで、タンパク質に変異が導入できる。
6) 小角散乱(法)
試料にX線や中性子などの量子ビームを照射し、角度が小さい範囲での回折のデータを用いて物質の構造情報を得る解析方法。例えば、溶液状態での試料の構造情報が得られるという特徴がある。
7) RecA
大腸菌からヒトに至るまで、ほとんどすべての生物がもっている普遍的なタンパク質の一つ。DNAの修復で重要な相同的組換え反応において中心的な役割を持つほか、DNAの傷の修復や突然変異の発生等にも深い関わりがある。分子の構造は多量体で、右巻きのらせんを形成する。
図1(白黒で簡略化)