(産学共同実用化開発事業(NexTEP)の成果)
2018/11/19 科学技術振興機構
ポイント
- 1細胞質量分析法は、これまで手動での吸引作業が必要で、再現性や処理効率の低さが課題となっていた。
- 今回、全自動の細胞内物質吸引装置を実現したことにより、ワンクリックで細胞中の狙った物質を吸引し、薬剤の薬理、局在、代謝、毒性の解析を大量に効率良く処理することができるようになった。
- 細胞内物質の吸引や質量分析に加え、創薬や医療などの幅広い分野の発展に貢献することが期待される。
JST(理事長 濵口 道成)は、産学共同実用化開発事業(NexTEP)の開発課題「共焦点画像1細胞創薬支援システム」の開発結果を成功と認定しました。
この開発課題は、理化学研究所 生命システム研究センター(QBiC)故 升島 努 教授らの研究成果を基に、平成26年8月から平成29年3月にかけて横河電機株式会社(代表取締役社長 西島 剛志、本社住所 東京都武蔵野市中町2丁目9-32、資本金434億105万円)に委託して、同社 計測事業本部 ライフサイエンスセンター(現 ライフイノベーション事業本部 バイオソリューションセンター)にて企業化開発を進めていたものです。
1細胞質量分析法注1)は、升島教授らによって発明された技術で、細胞を顕微鏡で観察しながらその変化を画像で追跡し、注目する細胞内小器官注2)を見たい時にナノスプレーチップ注3)で取り出し、ほぼそのまま質量分析を行うことができます。この手法は、疾患の分子機構の解明や細胞1つでの診断や個別化医療注4)に道をつけるものとして注目されています。しかし、従来の方法では、細胞を一つ一つ手動で吸引するため、その精度は作業者の熟練度に左右されていました。また、大量の細胞を処理するのにも不向きでした。そこで、1細胞質量分析法の実用化のために、細胞吸引の自動化や処理効率の向上に対する要望が高まっていました。
今回開発した技術は、細胞内物質を自動で吸引する装置です。本装置は、ユーザーがあらかじめ定義した条件に一致する細胞を装置が選び出し、指定された場所を自動で吸引します。従来、熟練者が顕微鏡下で時間をかけて行っていた作業をパソコン上でワンクリックで行うことができ、1時間あたり22検体と手作業の4倍強を取得し、狙った細胞の特定部位を高精度で確実に、かつ高効率に取り出すことが可能となりました。
微量の細胞内物質の吸引を自動化することによって、1細胞質量分析法が実用化に向けて大きく前進します。さらに、従来の多細胞平均による解析を補完する1細胞解析は創薬の低コスト化、効率化をもたらす最新の技術として期待されています。
産学共同実用化開発事業(NexTEP)は、大学等の研究成果に基づくシーズを用い、民間企業が単独で事業化することが困難な、開発リスクが高く規模の大きい開発を支援し、実用化を後押しする事業です。
詳細情報 https://www.jst.go.jp/jitsuyoka/
<背景>
1細胞質量分析法は従来の多数の細胞の平均値をとる従来の方法と異なり、詳細で正確な解析が行えるため、国内外の製薬企業から注目されています。これまで、理化学研究所と製薬企業との間で1細胞質量分析に関する共同研究が数多く行われてきました。しかし、実用上の問題として、細胞の中から目的の物質を取り出すのは簡単ではありませんでした。無数の細胞を顕微鏡で観察し、その中から特定の細胞を探すことはユーザーの主観によるところが大きく、同時に、吸引する細胞の箇所もユーザーの判断に委ねられます。このことから、吸引した試料の性質の再現性に問題がありました。また、吸引する際の吸引量を決める吸引圧力、吸引時間もユーザーの手で決められるため、定量性にも問題がありました。これらの問題のため、1細胞質量分析法は、大量の細胞を統計学的に処理するまでには至らず、研究的な利用に留まっていました。1細胞質量分析法の実用化のためにも、安定的に、再現性良く検体試料を制作する装置の開発が望まれてきました。
<開発内容>
従来製品の問題点を克服するために、以下の3つの技術を組み合わせて、自動吸引装置を開発しました。
1.細胞の画像を解析し、解析の結果に基づいて吸引対象を選択する技術
2.選択した細胞の吸引したい部位を高精度で捕捉する技術
3.ワンクリックで吸引を行うソフトウエア
1.細胞の画像を解析し、解析の結果に基づいて吸引対象を選択する技術
HCA手法注5)を用いて、細胞の顕微鏡画像を解析し、その結果に基づいて吸引対象を選択します。具体的には、細胞を顕微鏡で撮影しその画像から細胞の特徴量、例えば、細胞の面積、周囲長、真円度、発現した蛍光の明るさなどを算出します。これらの特徴量は、細胞への医薬化合物投与に対応した変化を示すため、特徴量という客観的な基準によって、目的とする細胞を特定し、吸引する検体の再現性を確保します。実際の装置では、注目する特徴量を1つか2つ抽出して、それを縦軸と横軸にしてグラフ化します。グラフ上の特徴量分布を見ながら、自動で吸引細胞を決定することができます(図1)。
HCA手法は、横河電機が以前に開発した自社技術であり、本プロジェクトでは、その技術を吸引装置における細胞の選択に応用しました。
2.選択した細胞の吸引したい部位を高精度で捕捉する技術
一般的に細胞の大きさは直径数μm~十数μm程度で、生きた細胞は培養容器の底面に貼り付いています。従って細胞質の層を捉えて穿刺し、細胞の中の物質を吸引するためにはターゲットとなる細胞部位と吸引チップの先端位置の両方をミクロンオーダーの精度で正確にコントロールし続ける必要があります。
横河電機は自社の持つ共焦点顕微鏡注6)の技術やHCA手法により細胞の形態を3次元で解析し、吸引部位の位置をミクロンオーダーの精度で特定することができました。また、チップの先端位置の検出については、本プロジェクトの中で、新たに画像強度法注7)を開発し、吸引チップの先端位置を1μm以下の精度で検出できるようになりました。この技術は特許出願しています。
細胞の3次元計測と吸引チップ先端の位置検出を高精度で行うことによって、両方の位置関係を正確にコントロールし、目的の物質を吸引することが可能となりました(図2、図3)。
3.ワンクリックで吸引を行うソフトウエア
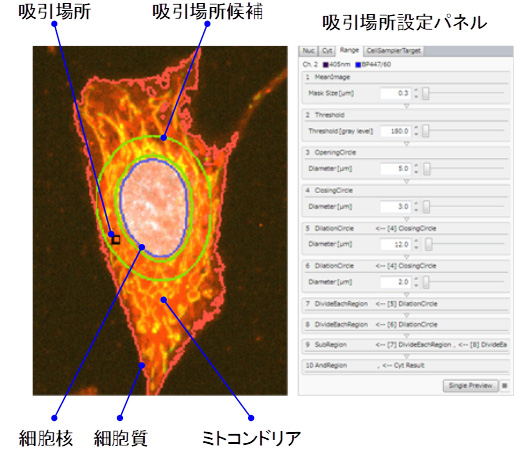
従来、吸引場所の選定は細胞核の周辺部で細胞質が豊富にある位置を熟練者が経験的に顕微鏡下の目視で行っていました。また、細胞核は比較的固いため、チップが当たるとしなるなど吸引には向きません。本装置では、このような情報を数値化し、吸引の自動設定機能を開発しました。具体的には、細胞質が豊富な場所は蛍光マーカーの輝度が高いことに着目し、熟練者の経験を基に、吸引位置を「核から一定距離の帯状の領域内で、細胞質の明るさが最も高い位置」と定義してソフトウエアを開発しました。吸引場所のほか、吸引圧力、吸引時間などの条件設定もできるようにしているほか、ユーザーは注目する細胞を目視しながら吸引したい場所をパソコン上でワンクリックで吸引することができます(図4)。
これらの技術を盛り込んだ自動吸引機能により、検体の取得効率が大幅に向上し、1時間あたり22検体の取得が可能になりました。
<期待される効果>
吸引の自動化により再現性の高い検体が取得できるようになったことで、1細胞質量分析法の実用化や新薬の開発、個別化医療など幅広い分野での利用が期待されます。また、質量分析以外では、細胞を丸ごと吸引してのmRNA解析や取得した検体を細胞へ注入することにも応用が可能であり、幅広い分野での貢献が期待されます。
<参考図>
![]()
図1 「ワンクリックで吸引を行うソフトウエア」画面
画面「特徴量分布図」にある個々のドットは細胞に対応します。例えば、薬剤に反応してより広い範囲で強く光っている細胞を選択したい場合、分布図上で所望のドットを選びクリックすることで吸引する細胞を決定できます。特徴量分布図上で予め設定した特徴量の範囲で吸引細胞を自動設定することも可能です。
![]()
図2 細胞内物質の吸引過程
断面図に細胞質を吸引している過程(吸引チップは透明のため、映らない)。
![]()
図3 細胞内物質吸引の例
上段左:吸引前の細胞 上段中央:穿刺直前 上段右:穿刺直後
下段左:吸引中 下段中央:チップ引上げ後 下段右:吸引後のチップ内
![]()
図4 吸引場所の自動設定
細胞核の周りで、細胞質が集中しているところを吸引する例。
<用語解説>
- 注1)1細胞質量分析法
- 顕微鏡で細胞の動きを観察しながら、注目したい細胞内小器官を見たい瞬間に、ナノスプレーチップと呼ばれる特殊な細管で捕捉吸引し、取り出した数百フェムトリットル(fL)の細胞内成分を質量分析にかけ、数千種の分子のピークを得ることができる分析方法。従来の多細胞の平均値解析に対して、本手法では、細胞1個レベルで、細胞中の分子変化を網羅的に検出することができる。疾患の分子機構の解明、細胞1個での診断や個別化医療にも道をつける手法として注目されている。
- 注2)細胞内小器官
- 細胞の内部に含まれる構造体の総称。遺伝情報の保存と伝達を行う細胞核、エネルギー生産を担うミトコンドリア、光合成にかかわる葉緑体などが含まれる。
- 注3)ナノスプレーチップ
- 先端内径がφ3μm程度、外径φ5μm程度のガラス細管。電極となるため、外周一部は伝導性材料でコートしている。
- 注4)個別化医療
- 患者の個人差に配慮して、各個人に適した治療を行う医療。遺伝子情報や病状に合わせて、その患者に有効な薬剤や治療法を選択する。テーラーメード医療、オーダーメード医療ともいう。
- 注5)HCA(High content analysis)手法
- 細胞に薬の候補となる化合物を投与し、その細胞を顕微鏡を介して蛍光画像で観察し、画像処理、画像解析を行い、化合物の薬効や毒性などを解析する分析手法。
- 注6)共焦点顕微鏡
- 光源から照射された光が試料表面に焦点を結ぶとき、その反射光も検出器上で焦点が合うように設計された顕微鏡。非合焦時の光は検出器に届かないので、焦点の合った部分だけが際立って明るく観察される特徴がある。ノイズの少ない高精細な細胞画像の取得が可能で、信頼性の高い解析結果を得ることができる。また、焦点距離を変えながら測定した結果をつなぎ合わせることで、対象の三次元的な形状を測定することができる。
- 注7)画像強度法
- 吸引チップを顕微鏡の対物レンズに近づけながら、その先端の反射像を取得すると、先端が対物レンズの焦点にあった時、最も明るい画像が得られる原理を利用し、吸引チップの先端位置を割り出す手法。本装置の顕微鏡は共焦点方式であるため、高さ方向の分解能が高く、チップの先端位置を1μm以下の精度で検出できる。
<お問い合わせ先>
<開発内容に関すること>
横河電機株式会社 ライフイノベーション事業本部 バイオソリューションセンター
<JST事業に関すること>
大竹 利也(オオタケ トシヤ)
科学技術振興機構 産学共同開発部