化学合成品により再生医療の大幅なコストダウンへ
2020-04-02 東京大学,川崎市産業振興財団 ナノ医療イノベーションセンター,科学技術振興機構
ポイント
- 組織の再生や保護作用を示す細胞増殖因子の代替化合物を開発し、モデルマウスにおいて肝炎の抑制効果を示すことを実証した。
- 生体環境において安定に存在し、高い生理活性を示す細胞増殖因子代替化合物を、生体物質であるデオキシリボ核酸(DNA)に基づいて設計可能であることを初めて報告した。
- 化学合成可能な細胞増殖因子代替化合物は、再生医療のコストダウンや安全性の向上を実現する新しい医薬品の候補として期待される。
細胞増殖因子は、組織の再生や保護、ES/iPS細胞などの幹細胞の分化を促すたんぱく質であり、再生医療分野への応用が広く期待されています。しかし、細胞増殖因子は熱的に不安定な物質であり厳密な品質管理が必要とされること、また、製造に生物を用いた高コストな生産過程を要することが応用面における大きな課題となっています。
東京大学 大学院工学系研究科の植木 亮介 助教、内田 智士 特任助教、オラシオ・カブラル 准教授、山東 信介 教授ら、川崎市産業振興財団 ナノ医療イノベーションセンターの藤 加珠子 研究員らの共同研究グループは、生体物質であるデオキシリボ核酸(DNA)注1)のみから構成される肝細胞増殖因子の代替化合物を開発し、モデルマウスにおいて肝炎の抑制効果を示すことを報告しました。DNAは化学合成により安価に大量生産可能であり、非常に熱安定性の高いマテリアルであるため、細胞増殖因子代替化合物として望ましい性質を持ちます。このような特性から、将来的には再生医療の大幅なコストダウンや安全性の向上につながる可能性が期待できます(図)。
本研究成果は、2020年4月1日(米国東部夏時間)に米国科学振興協会(AAAS)が出版する科学誌「Science Advances」オンライン版に掲載されます。
本研究は、JST 戦略的創造研究推進事業 チーム型研究(CREST)の研究領域「新機能創出を目指した分子技術の構築」(研究総括:山本 尚 中部大学 教授)の研究課題名「超高感度化分子技術により実現する巨視的ケミカルバイオロジー」(JPMJCR13L4)、公益財団法人 上原記念生命科学財団研究助成金、科学研究費助成事業 若手研究(B)(17K14512)の支援を受けて行われました。また、藤 加珠子 研究員はJST センター・オブ・イノベーション(COI)プログラム(JPMJCE1305)の支援を受けて本研究に参加しました。
<発表内容>
細胞増殖因子は、細胞の増殖や分化を制御する生理活性物質として知られており、その特性から近年の再生医療において大きな注目を集めています。例えば、肝臓の保護・再生に関与する肝細胞増殖因子(HGF)は、組織や神経の保護・再生を促す目的で、筋萎縮性側索硬化症(ALS)、脊髄損傷、肝硬変など治療への応用が検討されています。また、ES/iPS細胞など多能性幹細胞の培養や分化誘導にも用いられており、今後、再生医療における細胞増殖因子の重要性はますます高まると考えられています。しかしながら、たんぱく質注2)から構成される細胞増殖因子はマテリアルとしての観点からいくつかの問題点を抱えています。第一に、たんぱく質の多くは生物を利用した過程により製造されるため、コストが非常に高価となります。細胞増殖因子の市場価格(研究用試薬)は1マイクログラムあたり数百円-数千円であり、再生医療への応用や基礎研究の遂行における大きなボトルネックとなっています。第二に、たんぱく質である増殖因子は、複雑な形に折りたたまれた高次構造を形成することでさまざまな機能を発現します。しかし、外界の環境(熱や共存する物質)によって、この構造が不可逆的に破壊されると、その機能が失われてしまいます。このようなたんぱく質の不安定さによって、細胞増殖因子の保管や輸送の際には厳密な品質管理が求められます。
上記の問題点を解決するため、研究グループでは、生体物質であるデオキシリボ核酸(DNA)を用いて増殖因子の機能を模倣する物質の開発を行いました。肝細胞増殖因子(HGF)に着目し、細胞表層に存在するHGF受容体を認識・活性化するDNA配列(DNAアプタマー注3))の設計に成功しました。DNAは熱による構造変化を受けても、温度を低下させると元の構造に回復する性質があり、取り扱いが非常に容易です。また、化学的に大量合成できるため、製造価格(研究用試薬)は1マイクログラムあたり数十円程度に抑えられます。
このように細胞増殖因子の代替化合物として望ましい特性を持つDNAアプタマーですが、血中に存在する酵素によって速やかに分解されてしまうため、治療薬としての応用が大きく妨げられています。今回研究グループは、HGF様の活性を示すDNAアプタマーが独特の折りたたみ構造を形成することで、酵素による分解を大幅に抑制していることを見いだしました。血清含有溶液中において通常のDNA配列が速やかに分解されたのに対し、開発したアプタマーは24時間後においてもほぼ半数が残存していることが分かりました。さらに詳細な検討の結果、このアプタマーをマウスへ静脈注射した場合、一部は血液中での分解を回避して肝臓へ移行し、HGFと同様の生理作用を発現することが分かりました。HGFは肝炎・肝硬変などの難治性肝疾患の治療薬としての応用が検討されていたことから、肝炎モデルマウスにおいて開発したアプタマーの治療効果を評価しました。その結果、アプタマーを投与することによって肝炎の進行を抑制することができ、肝疾患の治療薬としての応用可能性が示されました。今後、さらなる構造最適化や、安全性の検証を行うことで、新たな再生医薬品の導出へとつながることが期待されます。
生命活動は生体内の無数の分子の相互作用の上に成り立っていますが、そのような分子の活動に着目した化学的アプローチ「ケミカルバイオロジー」は次世代医療に貢献する大きな可能性を秘めています。本研究成果は、生体成分であるDNAを用いた分子技術によって、再生医療のコストダウンや安全性の向上につながる新たな戦略を提案するものです。今回明らかになった、血液中で安定に存在して高い生理活性を発現する生体分子の設計指針を基に、細胞増殖因子代替化合物をはじめとしたさまざまな機能性分子の開発が進むことが期待されます。
<参考図>
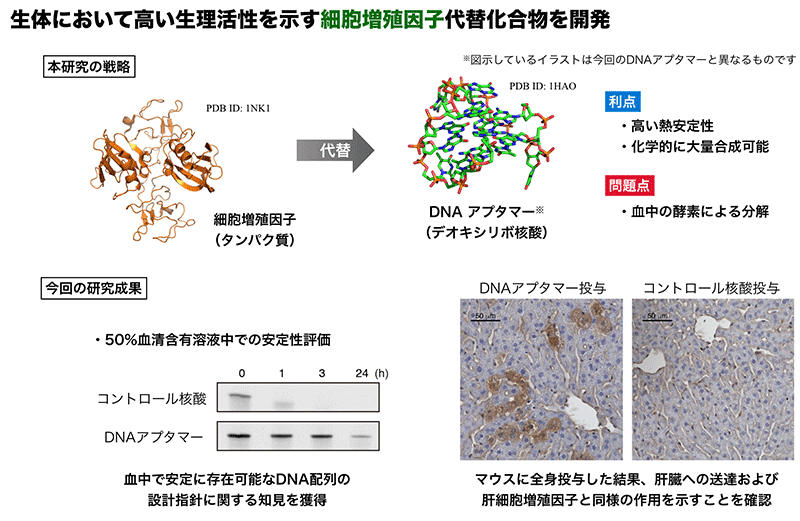 図 本発表の概要(From Sci. Adv. 6 : eaay2801 (2020). This work is licensed under CC BY-NC
図 本発表の概要(From Sci. Adv. 6 : eaay2801 (2020). This work is licensed under CC BY-NC
(http://creativecommons.org/licenses/by-nc/4.0/))
<用語解説>
- 注1)デオキシリボ核酸(DNA)
- 細胞の核内で二重らせん構造を形成しており、生体の設計図とも言える遺伝情報を保持する物質。アデニン(A)、チミン(T)、シトシン(C)、グアニン(G)と呼ばれる構造を持つ4種類の基本単位が連なることで構成されている。
- 注2)たんぱく質
- アミノ酸と呼ばれる20種類の基本単位が連なることで構成される生体物質。溶液中において、たんぱく質は複雑な形に折りたたまれた高次構造を形成し、さまざまな機能を発現する。しかし、外界の環境(熱や共存する物質)によって構造が不可逆的に破壊されると、その機能が失われてしまう。
- 注3)DNAアプタマー
- DNAもたんぱく質と同様、複雑な形に折りたたまれた高次構造を形成する。形成される高次構造によっては特定の分子を選択的に認識することができ、そのような特性を持つDNA配列をDNAアプタマーと呼ぶ。DNAアプタマーは、化学合成されたランダムDNA配列の中から、標的分子に結合したものを単離・増幅する進化工学的過程を繰り返すことによって取得することができる。
<論文タイトル>
- “A chemically unmodified agonistic DNA with growth factor functionality for in vivo therapeutic application”
- 著者名:Ryosuke Ueki, Satoshi Uchida, Naoto Kanda, Naoki Yamada, Ayaka Ueki, Momoko Akiyama, Kazuko Toh, Horacio Cabral, and Shinsuke Sando
- DOI:10.1126/sciadv.aay2801
- アブストラクトURL:https://advances.sciencemag.org/
<お問い合わせ先>
<研究内容に関すること>
植木 亮介(ウエキ リョウスケ)
東京大学 大学院工学系研究科 化学生命工学専攻 助教
山東 信介(サンドウ シンスケ)
東京大学 大学院工学系研究科 化学生命工学専攻 教授
<JST事業に関すること>
嶋林 ゆう子(シマバヤシ ユウコ)
科学技術振興機構 戦略研究推進部 グリーンイノベーショングループ
<報道担当>
科学技術振興機構 広報課