2024-01-04 名古屋工業大学,科学技術振興機構
発表のポイント
〇 テトラフルオロスルファニル(SF4)アセチレンの合成に成功
〇 50種類を超える新規なSF4アセチレン物質を合成
〇 SF4アセチレンから様々なSF4化合物に変換可能
〇 PFAS代替品や環境に配慮した農薬の開発研究に拍車
概要
フッ素(*1)を有機分子に導入することで、化学的安定性などの特定の性質が付加されることが知られており、有機フッ素化合物は医薬品や殺虫剤などの薬品類から、フライパン、エアコン、冷蔵庫のガスなどの日常製品まで幅広い用途で活用されています。しかし近年、環境への懸念から有機フッ素化合物の規制が拡大されつつあります。特にPFAS(*2)の使用規制が進む中、PFASに該当しない環境性に優れた代替品の需要が高まっています。
名古屋工業大学大学院工学研究科共同ナノメディシン科学専攻及び工学専攻(生命・応用化学領域)の柴田哲男教授らの研究グループは、テトラフルオロスルファニル(SF4)化合物が、PFASに代わる環境負荷の低い有機フッ素化合物になりうると考え、その合成素子であるSF4アセチレン化合物群の画期的な合成手法の開発に成功しました。本研究では、銅(Cu)触媒と芳香族ジアゾニウム塩を使用したラジカル反応(*3)を応用することで、様々なSF4アセチレン誘導体を短時間で合成することができます。この手法は基質適応性が高く、多彩な官能基で修飾されたSF4アセチレン化合物の合成に応用できます。さらに得られたSF4アセチレン化合物は、より複雑なSF4化合物群に分子変換が可能です。SF4化合物はPFAS規制対象外の有機フッ素化合物です。この成果により、PFAS代替品の開発研究が進み環境に優しい有機フッ素化合物の合成が実現することが期待されます。
この研究成果は、2023年12月31日に総合科学誌「Advanced Science」のweb版で公開されました。
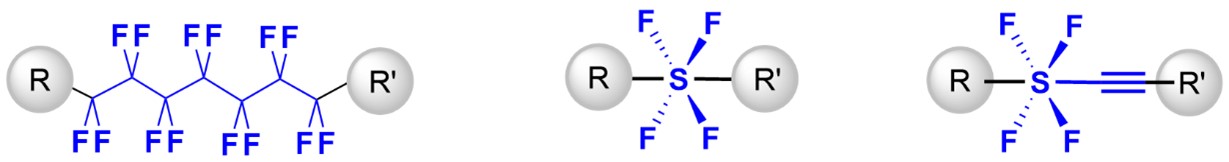
PFAS類の部分構造(左)と柴田らが開発したSF4化合物およびSF4アセチレンの構造(中央、右)
研究の背景
フッ素原子は水素に次ぐ小さな原子半径と最大の電気陰性度を持ち、有機分子にフッ素を組み込むことで、化学構造を変えずに物性を大きく変化させることができます。この性質は、医薬品、農薬、エアコン冷媒、高分子樹脂など、様々な分野で重要視されています。しかし、高度にフッ素化されたPFOS(*4)やPFOA(*5)などは、自然環境に放出されると分解されずに残り、生物体内に蓄積されることが明らかになっています(図1)。EUでは、PFOSやPFOAに限らず、全てのパーフルオロアルキル化合物やポリフルオロアルキル化合物がPFASとして規制される動きが広がっています。
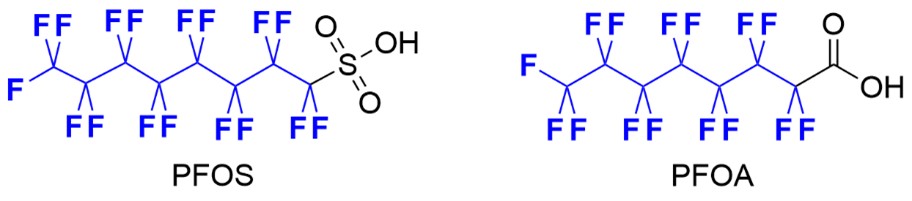
図1.PFOSおよびPFOAの化学構造
このような状況の中で、本研究グループは6価の硫黄原子(S)に4つのフッ素(F)原子が結合したテトラフルオロスルファニル(SF4)化合物に注目しました。SF4部位は強力な電子求引性と高い脂溶性を有し、有機化合物に組み込むことで、PFASに類似した特性を示しますが、難分解性の原因となるフルオロアルキル部位を持ちません。このため、SF4化合物はPFAS規制の対象外でありながら、環境に優れたPFAS代替品として機能する可能性があります。
SF4化合物は、分子設計上の大きな特徴を持ち、SF4部位を介して、連結距離3.66Å(オングストローム、1Åは10⁻¹⁰m)の非共役系直線構造で2つの独立した化合物部位を結びつけることができます。さらに、SF4基とアセチレン(*6)を直接組み合わせたSF4アセチレンでは、6.23Åの直線構造で2つのユニットを結びつけることができます。なおこの場合は、共役系(*7)と非共役系のハイブリッド型になります(図2)。
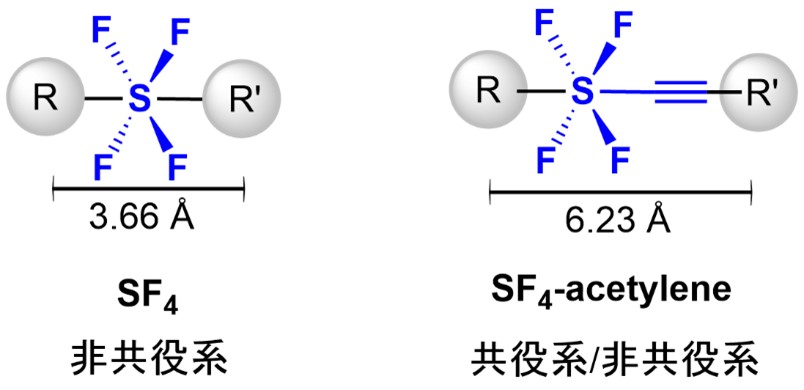
図2.SF4化合物およびSF4アセチレンの化学構造とその結合距離
直線構造は機能性分子や医薬品に見られる部分構造であり、例えばパラ置換ベンゼン(連結距離5.86Å)やアセチレン(連結距離4.13Å)が共役系直線構造の代表的な例です。近年では、ビシクロ[1,1,1]ペンタン(BCP、連結距離4.91Å)やキュバン(連結距離5.73Å)といった非共役系直線連結素子が開発されており、直線的な分子構造を持つ有機化合物の合成研究が活発化しています(図3)。
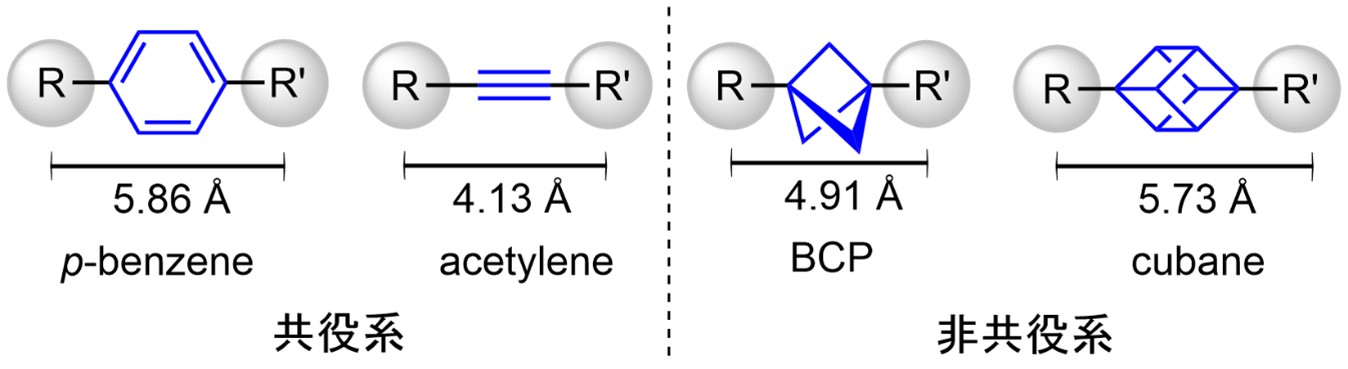
図3.直線連結素子として用いられる構造と結合距離
SF4化合物は半世紀以上前から報告されていますが、その合成手法は限られており、SF4化合物を用いた研究はほとんど行われていませんでした。本研究グループは以前より、SF4アセチレンを用いた合成反応を報告していますが、アセチレン末端に様々な官能基を持つSF4アセチレンの合成が容易ではありませんでした。今回、Cu触媒と芳香族ジアゾニウム塩を組み合わせたラジカル型クロスカップリング反応(*8)を応用することで、多種多様なSF4アセチレン誘導体を、簡便に高収率で合成する手法を開発しました(図4)。
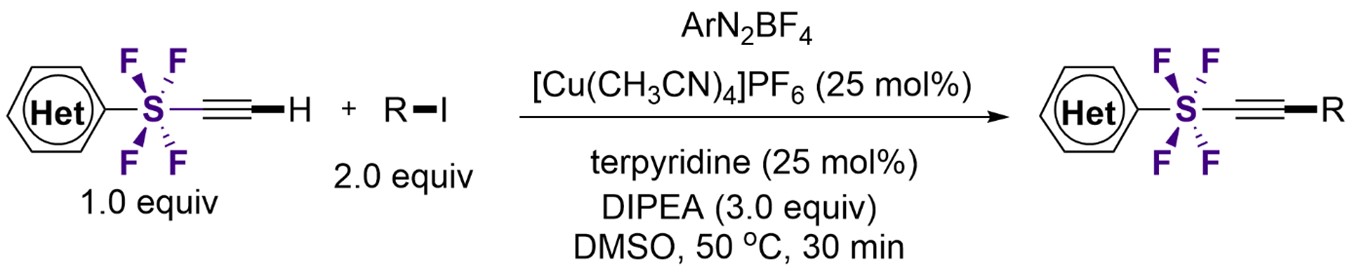
図4.今回開発されたSF4アセチレンとヨウ化アルキルとのクロスカップリング反応
研究の内容・成果
本研究グループが開発したラジカル型クロスカップリング反応は、以下のように実施できます。末端が水素のSF4アセチレンをCu触媒、有機塩基、配位子、芳香族ジアゾニウム塩の存在下でヨウ化アルキルと反応させることで、わずか30分の反応時間で、SF4アセチレンがアルキルヨウ化物と効果的にクロスカップリングし、末端に様々な官能基を装備した新しいSF4アセチレン化合物へと誘導できます。通常のアセチレン化合物とは異なり、SF4アセチレンはSF4基の強力な電子求引性により、アセチレン末端のC-H結合が活性化されています。そのため、穏やかな条件下で迅速にC-H結合の脱プロトン化が起こり、Cu(I)アセチリドが生成します。この後、Cu(I)アセチリドからジアゾニウム塩への一電子移動(SET)により窒素が押し出されると、アリールラジカルとCu(II)-アセチリド中間体が生成されます。アリールラジカルは速やかにヨウ化アルキルを脱ヨウ素化し、アルキルラジカルを形成します。そして、生じたアルキルラジカルはCu(II)-アセチリドと酸化的付加反応してCu(III)種を生成します。この後、この還元的脱離反応の過程で直線構造を持つSF4化合群が合成され、同時にCu(I)触媒が再生され、触媒サイクルが終了します(図5)。
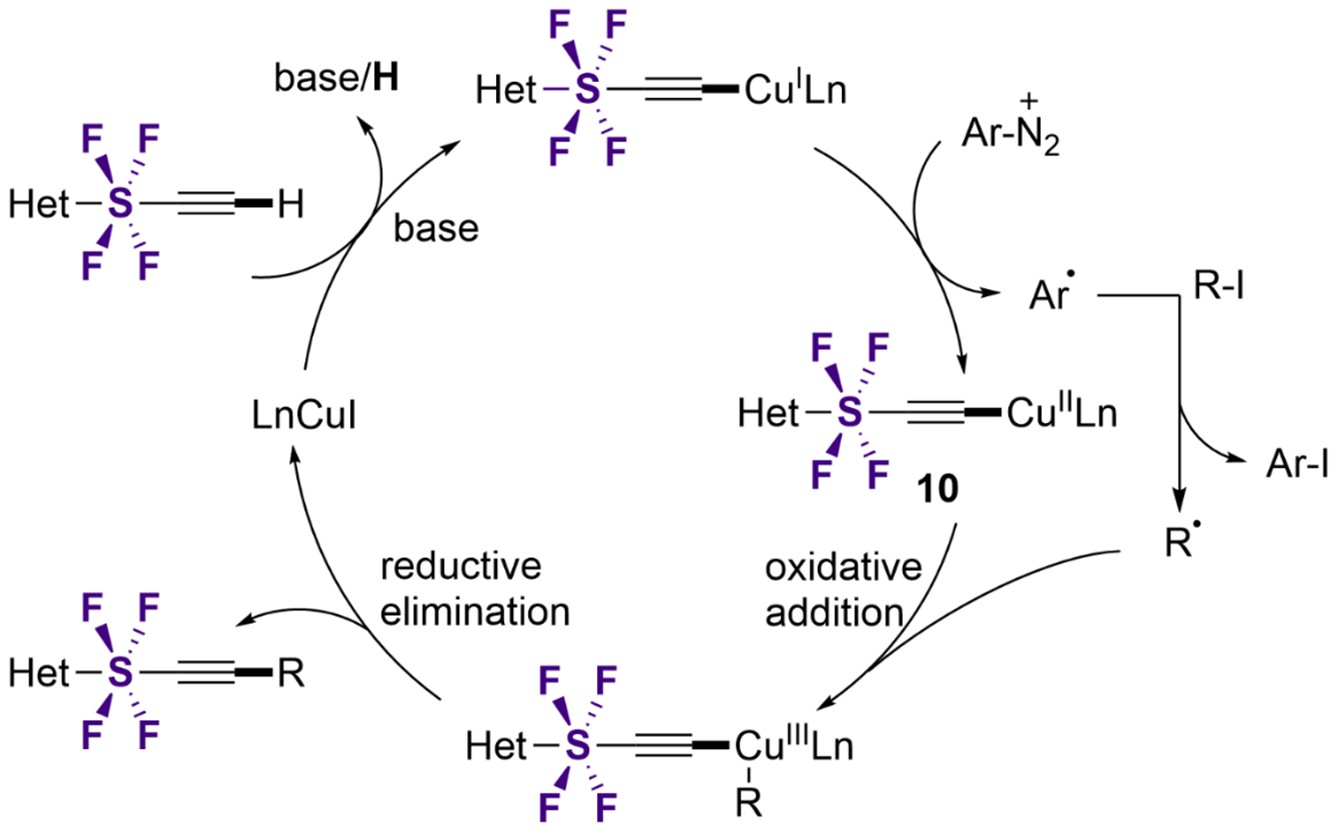
図5.SF4アセチレンとヨウ化アルキルとのクロスカップリング反応の作業仮説
この分子変換手法の基質適応性は非常に広範であり、1級、2級、および3級のヨウ化アルキル類で実施可能です。複素環、カルボニル基、アルコール、オレフィンなどの官能基に対する適合性も非常に高く、50種類以上の実施例によりその広範な基質適応性が実証されています(図6)。また、本研究で得られるSF4アセチレン化合物は、ニトロンとの1,3-双極子付加環化やアジドとのクリック反応を行うことで、2つの独立した複素環がSF4基で直線的に結合した物質へ化学変換が可能です(図7)。得られたSF4化合物は、環境に適応した農薬候補として魅力的な特性を持っています。
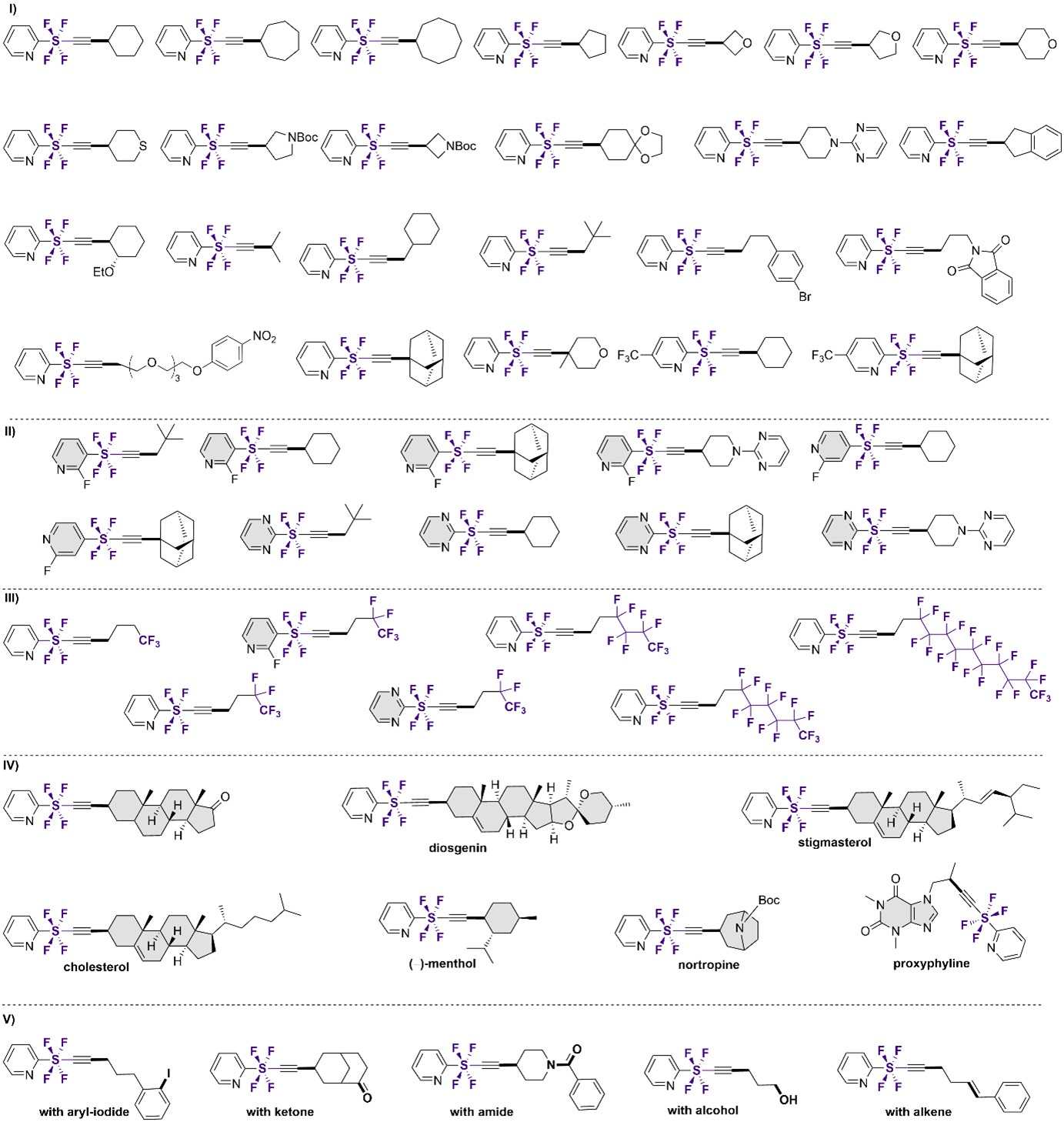
図6.本手法で合成されたSF4アセチレン化合物群
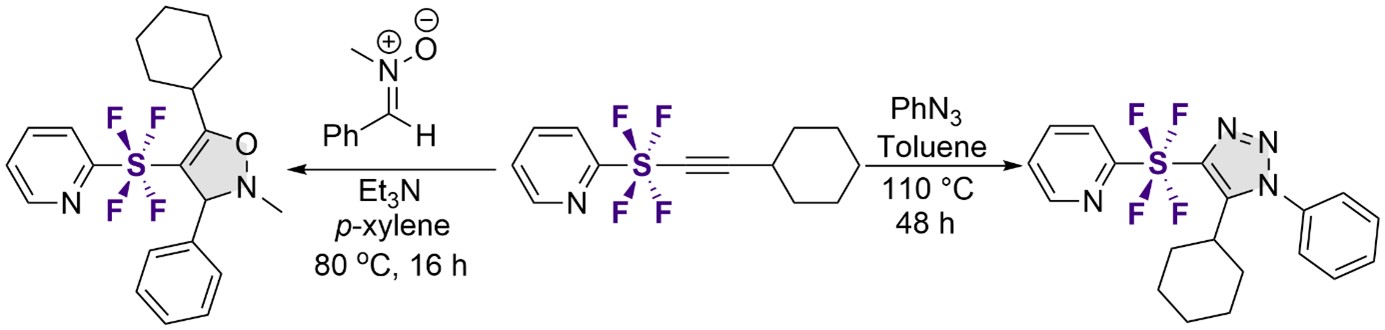
図7.ニトロンとの1,3-双極子付加環化(左)、アジドとのクリック反応(右)
社会的な意義
PFAS規制に伴い、環境保護が進む一方、私たちの生活や多くの産業が影響を受けることが懸念されています。このSF4化合物を用いた新しい合成技術を産業界が取り入れることで、PFAS規制の制限を受けることなく、環境に配慮した製品開発を大きく進めることが可能になります。このことは、産業界や一般の人々にとって、革新的かつ持続可能な解決策を提供するものとなります。
今後の展開
SF4化合物を用いた製品開発は、産業のパラダイムを変える可能性を秘めています。これは環境に優しい農薬やPFAS代替品、そしてSF4系のフッ素高分子樹脂など、多岐にわたる応用分野における技術革新をけん引するものです。本研究グループは、SF4化合物の可能性を最大限に引き出すため、新たな応用方法や革新的な製品の開発に向けて積極的に取り組んでおり、産業界との共同研究への発展を目指しています。
本研究は、JST戦略的創造研究推進事業(CREST)、研究領域「分解・劣化・安定化の精密材料科学」(研究総括: 高原 淳(九州大学 ネガティブエミッションテクノロジー研究センター 特任教授)における研究課題「フッ素循環社会を実現するフッ素材料の精密分解」(研究代表者: 柴田 哲男)(課題番号JPMJCR21L1)の支援を受けて実施しました。
論文情報
論文名: Expanding the Frontier of Linear Drug Design: Cu-Catalyzed Csp-Csp3-Coupling of Electron-Deficient SF4-Alkynes with Alkyl Iodides
著者名: Srikanth Reddy Narra, Muhamad Zulfaqar Bacho, Masasi Hattori, and Norio Shibata*
*責任著者
掲載誌: Advanced Science
Journal link: http://doi.org/10.1002/advs.202306554
掲載日: 2023年12月31日
用語解説
1. フッ素:元素記号「F」を持つ元素で、非金属元素の1つです。水素に次いで小さな原子半径と非常に強い電気陰性度を持っており、有機化合物の構造に組み込むと物質の性質を顕著に変化させることができます。特に化学的安定性に優れ、医薬品や農薬、エアコンのガス、工業製品などの製造に広く利用されています。これは、炭素(元素記号「C」)とフッ素との化学結合(C-F結合)は化学的に不活性であることが大きな要因の1つです。
2. PFAS:Per- and Polyfluoroalkyl Substances(パーフルオロアルキル化合物およびポリフルオロアルキル化合物)の略称です。PFASはフッ素原子と炭素原子から構成される有機化合物の総称であり、耐薬品性、不燃性、防水性や撥油性などの特徴を持つことから、暮らしに関わる広範囲な製品で使用されています。しかし、高い安定性のため環境中での分解が難しいうえ、生物に取り込まれると蓄積されることから、環境や健康に悪影響を及ぼすことが知られています。
3. ラジカル反応:ラジカルと呼ばれる高い反応性を持つ化学種が関与する反応です。紫外線や高温下で実施すると反応制御が困難でありましたが、近年は遷移金属触媒や光触媒などの存在下で温和な条件で選択的な部位でラジカル反応を実施できるようになっています。
4. PFOS:Perfluorooctanesulfonic acid(パーフルオロオクタンスルホン酸)の略称です。優れたはっ水性やはつ油性を持ち、様々な工業製品に使われていました。環境中で分解されにくく生物体内に蓄積されることが問題視され、残留性有機汚染物質に関するストックホルム条約(POPs条約)により製造・使用が制限されています。
5. PFOA:Perfluorooctanoic acid(パーフルオロオクタン酸)の略称です。PFOSと同様の性質を持ち、産業製品に利用されていましたが、ストックホルム条約で規制対象となっています。
6. アセチレン:2つの炭素原子が三重結合で結ばれた、分子式がC2H2の炭化水素です。三重結合部位や末端のC-H部位を足がかりとした、化学変換反応が可能です。様々なアセチレン誘導体が報告されており、いずれも優れた合成素子として有機合成化学で使用されています。
7. 共役系:多重結合(二重結合または三重結合)と単結合が交互に位置する構造。
8. クロスカップリング反応:有機化合物の合成において、1つの異なる化合物間で特定の化学結合を形成する反応です。C-C結合やC-ヘテロ原子結合の形成反応が可能で、鈴木―宮浦カップリングや園頭カップリングなどが知られています。異なる有機分子同士を結びつける反応で、遷移金属を触媒に用いる場合が多く見られます。
お問い合わせ先
研究に関すること
名古屋工業大学大学院工学研究科
教授 柴田 哲男
JST事業に関すること
科学技術振興機構 戦略研究推進部 グリーンイノベーショングループ
安藤 裕輔
広報に関すること
名古屋工業大学 企画広報課
科学技術振興機構 広報課