2024-04-17 東京大学
発表のポイント
- 約100ナノメートルの世界最高の空間分解能を有する中赤外顕微鏡の開発に成功し、細菌内部の生体分子の分布を観察することに成功しました。
- 単一の対物レンズを用いた開口合成イメージング法を新たに開発することにより、超解像中赤外顕微鏡である中赤外フォトサーマル顕微鏡の空間分解能を大幅に向上しました。
- 微細な構造を持つ物質の非接触、非破壊、かつ非標識での分子振動イメージングが重要な役割を果たす生物学、医学、材料科学などの分野での幅広い利用が期待されます。
中赤外フォトサーマル顕微鏡による細菌イメージングの概念図
発表概要
東京大学大学院理学系研究科の井手口拓郎准教授らは、約100ナノメートルの世界最高空間分解能を持つ中赤外顕微鏡の開発に成功しました。中赤外顕微鏡は、可視光を用いた通常の光学顕微鏡では捉えられない分子振動の空間分布を調べることができる特殊な顕微鏡ですが、空間分解能が通常の光学顕微鏡に比べて約10倍程度低い(数千ナノメートル程度)という原理的な欠点があります。そのため、細胞の観察など、細かい構造を見るのには不向きです。本研究では、原理限界を大幅に超える約100ナノメートルの空間分解能を持つ中赤外顕微鏡を開発し、細菌内部の生体分子の分布を観察することに成功しました。この技術により、微細な構造を持つ物質の非破壊、非標識、非接触での分子振動イメージングが可能になり、生物学、医学、材料工学などの分野での幅広い利用が期待されます。
発表内容
中赤外顕微鏡(注1) は、非破壊、非標識、非接触で物質の分子組成の空間分布を観察することのできる特殊な顕微鏡です。しかし、波長の長い中赤外光を用いた手法であるため、空間分解能は光の回折限界(注2)で決まる数千ナノメートル(数マイクロメートル)程度にとどまります。一方で、従来技術の空間分解能の限界を突破する中赤外フォトサーマル顕微鏡(注3)と呼ばれる技術が近年開発されています(関連情報「世界最高速の単一細胞中赤外顕微イメージングを実現」参照)。この顕微鏡は、中赤外光の吸収によって発生する熱による屈折率の変化を可視光の顕微鏡で検出することで、中赤外光の回折限界以下の空間分解能を実現する手法です。しかし、この技術の空間分解能の限界を引き出す手法は確立していませんでした。
東京大学大学院理学系研究科の井手口拓郎准教授らは、中赤外フォトサーマル顕微鏡に新たな技術を導入することで、約100ナノメートルの世界最高空間分解能の実現に成功しました。従来の中赤外フォトサーマル顕微鏡では、用いている対物レンズの開口数(注4)の低さと、パルス幅の長い中赤外光により生じる熱拡散という二つの原因により空間分解能が制限されていました。本研究では、高い開口数を持つ対物レンズを用いて高空間分解イメージングを実現する開口合成法(注5)を用いることで前者の問題を解決し(図1)、また、ナノ秒以下のパルス幅を持つ中赤外パルス光源を開発することで、後者の問題を解決することに成功しました。
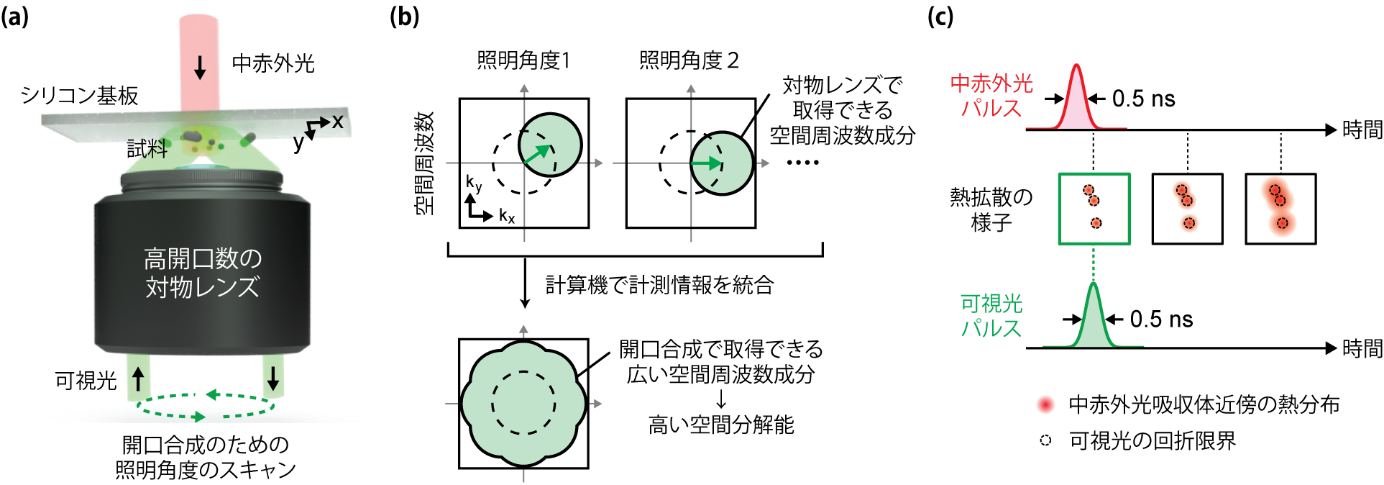
図1:単一の対物レンズを用いた開口合成手法に基づく中赤外フォトサーマル顕微鏡の概要
(a)単一の対物レンズを用いた中赤外フォトサーマル顕微鏡。試料を中赤外光を透過し可視光を反射するシリコン基板上に置くことにより、単一の対物レンズで開口合成を用いた中赤外フォトサーマル顕微鏡の実装が可能となった。(b)開口合成法の概略。異なる照明角度により広い空間周波数成分の情報を得ることで、高い空間分解能を得ることができる。(c)ナノ秒以下のパルス幅を持つ中赤外光パルスおよび可視光パルスを用いることで、中赤外フォトサーマル効果で生じた熱が広く拡散する前に計測を行うことができる。
これらの技術により、120ナノメートルの空間分解能を実現しました。さらに、可視光の波長と対物レンズの開口数を最適化することで、今後、100ナノメートル以下の分解能へと改善する余地があります。開発した顕微鏡を使用して、細菌内部のタンパク質や脂質といった生体分子の分布を非標識で可視化し、定量することに成功しました(図2)。
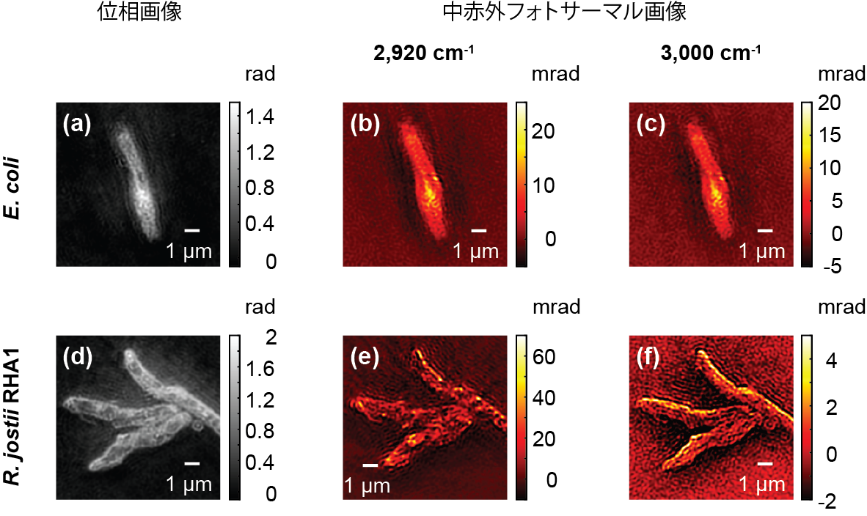
図2:高空間分解能中赤外フォトサーマル顕微鏡によるバクテリアのスペクトルイメージング解析
(a-c)Escherichia coli(大腸菌)と(d-f)Rhodococcus jostii RHA1の(a,d)位相画像、(b,e)2,920、(c,f)3,000 cm-1での中赤外フォトサーマル画像。R. jostiiRHA1では2つのフォトサーマル画像(e,f)の間で信号の空間分布が大きく変わっているが、E. coli(b,c)では大きな違いが見られないことから、2種類のバクテリアの間で細胞内の主要な分子種に違いがあることが推察される。特に、R. jostii RHA1では、2,920 cm-1での中赤外フォトサーマル画像(e)に脂質玉とみられる微小構造が確認できる。
従来のマイクロスコピーからナノスコピー(注6)へと進化した中赤外顕微鏡技術は、微細な構造を持つ物質の分子振動の分布を非破壊、非標識、非接触で分析することを可能にし、生物学、医学、材料工学などの分野での幅広い利用が期待されます。
*本研究は、東京大学大学院理学系研究科のVenkata Ramaiah Badarla特任助教(研究当時)、島田紘行特任研究員(研究当時)、小西邦昭准教授、東京大学先端科学技術研究センターの太田禎生准教授と共同で行われました。
〇関連情報:
「世界最高速の単一細胞中赤外顕微イメージングを実現」(2023/07/19)
論文情報
- 雑誌名
Nature Photonics論文タイトル
Mid-infrared wide-field nanoscopy著者
Miu Tamamitsu, Keiichiro Toda, Masato Fukushima, Venkata Ramaiah Badarla, Hiroyuki Shimada, Sadao Ota, Kuniaki Konishi and Takuro Ideguchi*
研究助成
本研究は、科研費「基盤研究(A)(課題番号:(20H00125、23H00273)」、科学技術振興機構(JST) 戦略的創造研究推進事業 さきがけ 「量子技術を適用した生命科学基盤の創出」研究領域 研究課題名「超高感度ラベルフリーイメージング法の開発」(課題番号:JPMJPR17G2)平成29年度採択(研究者:井手口 拓郎)、精密測定技術振興財団、光科学技術研究振興財団、中谷医工計測技術振興財団、UTEC-UTokyo FSI Research Grant Programの支援により実施されました。
用語解説
注1 中赤外顕微鏡
2,000-20,000ナノメートル(2−20マイクロメートル)程度の中赤外領域の波長を持つ光を用いた顕微鏡。物質を構成する各種分子は異なる波長の中赤外光を吸収して振動するため、中赤外顕微鏡を用いると分子振動特異的な空間分布画像を得ることができます。
注2 回折限界
光の回折現象により、この限界よりも小さな物体のイメージはぼやけて観測されます。この限界は、光の波長に比例し、レンズの開口数に反比例します。
注3 中赤外フォトサーマル顕微鏡
中赤外光の回折限界以下の空間分解能を実現できる中赤外顕微鏡。中赤外光の吸収で生じる熱により変化する屈折率変化を可視光の顕微鏡で定量することにより、可視光の回折限界で決まる空間分解能を実現できます。
注4 開口数
レンズが光を集める範囲を表す指標であり、この数値が大きい方が空間分解能が高くなります。
注5 開口合成法
異なる角度の照明による複数の顕微鏡計測で試料の空間周波数スペクトルの異なる成分を個別に計測し、これらを計算機上で統合することで、通常の顕微鏡計測よりも高い空間分解能の画像を取得する方法。
注6 ナノスコピー
100ナノメートル以下の空間分解能を有する顕微鏡計測。