2022-02-11 理化学研究所
理化学研究所(理研)環境資源科学研究センター機能有機合成化学研究チームのイリエシュ・ラウレアンチームリーダー、浅子壮美上級研究員らの研究チームは、新たに設計した「ルーフ配位子[1]」を持つイリジウム(Ir)[2]触媒[3]を用いて、芳香族炭化水素[4]の選択的な官能基化反応の開発に成功しました。
本研究成果は、医農薬品や機能性分子の選択的かつ効率的な合成手法の開発に貢献すると期待できます。
芳香族炭化水素を1工程で官能基化する反応の開発は、入手容易で単純な化合物の高付加価値化や複雑な医農薬品や機能性分子の迅速な合成につながることから、近年精力的に研究されています。しかしこれまでは、芳香族炭化水素に複数ある水素(H)原子を区別できず、生成物がオルト、メタ、パラ体[5]の混合物になってしまうという課題がありました。特に、芳香族炭化水素に官能基をメタ位選択的に直接導入することは困難でした。
今回研究チームは、金属触媒の配位子として知られる2,2′-ビピリジン[6]を3次元的に拡張した化合物に「屋根」を取り付けた配位子(ルーフ配位子)を設計し、Ir錯体と共に触媒として用いることで、さまざまな芳香族炭化水素のホウ素化反応[7]がメタ位選択的に進行することを見いだしました。このルーフ配位子/イリジウム触媒は、置換基から最も離れた反応点であるパラ位[5]を選択的にふさぐことで、1工程でのメタ位選択的反応を達成しました。本反応は、アルキルベンゼン、アニリン、フェノール誘導体などの芳香族炭化水素のメタ位選択的官能基化に利用できるほか、複雑な医薬品分子の官能基化もメタ位選択的に行えます。
本研究は、科学雑誌『Science』(2月11日号)の掲載に先立ち、オンライン版(2月10日付:日本時間2月11日)に掲載されます。
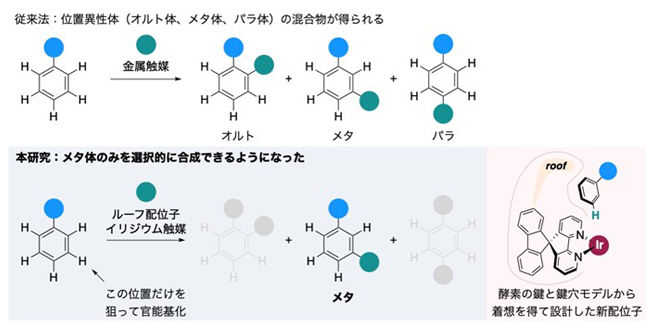
ルーフ配位子を持つイリジウム触媒を用いた芳香族炭化水素のメタ位選択的官能基化
背景
金属触媒を用いて芳香族炭化水素を1工程で官能基化(直接官能基化)する反応は、複雑な医農薬品や機能性分子の迅速な合成を可能とすることから、近年精力的に研究・開発されています。しかし、この直接官能基化では、化合物中に複数ある炭素-水素結合(C-H結合)を識別し、望みの位置だけを官能基化できるかという「位置選択性」に課題があります。もしも、金属触媒が炭素-水素結合を区別できずにさまざまな位置でランダムに反応すると、生成物は分離が困難な異性体の混合物になるため、合成において有用とはいえません。
位置選択性の制御には「立体制御」が用いられ、一般に芳香族炭化水素のかさ高い置換基の近傍位の反応点をふさぐという戦略がとられます。そのため、例えば、一置換ベンゼンのオルト位は一般に反応性が低くなっています。しかし、このような従来の立体制御は近傍位の制御に限られるため、より遠隔位にあるメタ位とパラ位の区別は困難でした。
研究手法と成果
研究チームは、芳香族炭化水素のホウ素化反応において、遠隔位の立体環境を制御するための戦略として、平面的な構造を持つ2,2′-ビピリジンを3次元的に拡張したスピロビピリジン(SpiroBpy)に「屋根」となるBPin(ピナコールボリル)基を取り付けた配位子を持つ金属触媒を設計し、この配位子を「ルーフ配位子」と名付けました。
ルーフ配位子は、金属(本研究ではイリジウム:Ir)への配位部位から離れた所に立体障害となる屋根を持つため、基質となる芳香族炭化水素の遠隔位のメタ位とパラ位を区別できます(図1)。すなわち、芳香族炭化水素のパラ位置換基の接近だけを選択的に防ぐことができる一方で、メタ位置換基とはほとんど相互作用しないために基質が接近できます。これは、特定の配置で接近する基質だけを認識する酵素の鍵と鍵穴モデル[8]に似ています。その結果として、一置換ベンゼンのメタ位の炭素-水素結合のみが選択的にIr触媒に切断され、基質にホウ素官能基を導入できます。
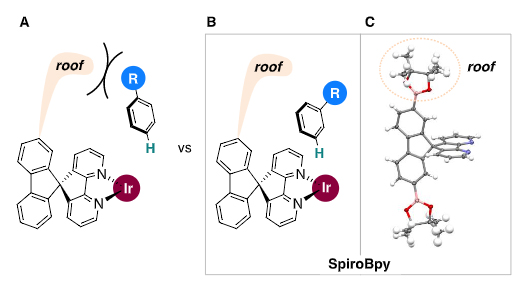
図1 ルーフ配位子を持つイリジウム触媒の設計
A:ルーフ配位子の屋根が芳香族炭化水素のパラ位置換基(R)の接近を阻止するため、パラ位水素(H)はイリジウム(Ir)と相互作用できない。
B:ルーフ配位子の屋根と芳香族炭化水素のメタ位置換基はほとんど相互作用がないため、メタ位水素はイリジウムと反応できる。
C:単結晶X線構造解析によって決定したルーフ配位子(SpiroBpy)の分子構造。
この触媒系を利用すると、アルキルベンゼン、アニリン、フェノール、アリールシラン、アリールホスホン酸エステル誘導体などの比較的単純な芳香族炭化水素をメタ位選択的にホウ素化できるだけでなく、カラミフェンのような複雑な医薬品分子のホウ素化も可能です(図2)。
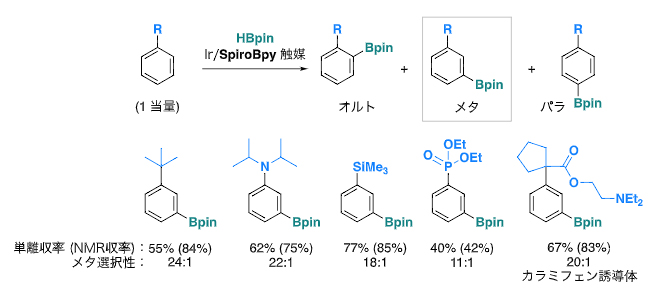
図2 ルーフ配位子を持つイリジウム触媒を用いた芳香族化合物のメタ位選択的ホウ素化反応
上段:ルーフ配位子(SpiroBpy)を持つイリジウム触媒(Ir/SpiroBpy触媒)を用いて、一置換ベンゼンにBpin基(ピナコールボリル基)を導入するホウ素化反応。Bpin基が一置換ベンゼンのオルト位、メタ位、パラ位の3種類の位置に導入される可能性がある。
下段:左からアルキルベンゼン、アニリン誘導体、アリールシラン誘導体、アリールホスホン酸エステル誘導体、カラミフェン誘導体のホウ素化反応の例。比較的高い収率で、非常に高いメタ位選択性を示すことが分かった。収率は、精製操作後の単離収率とカッコ内に反応粗生成物のNMR(核磁気共鳴)収率を示す。メタ選択性はメタ体とパラ体の比率である。
特に、ケイ素置換基で保護されたフェノール誘導体のメタ位官能基化は合成において有用です。本反応は、21:1の高いメタ位選択性で対応するホウ素化生成物を与えます(図3左)。生成物のホウ素化合物は、既知の変換反応によりさまざまな官能基へと変換でき、メタ位ホウ素化合物を基点としてヨウ素(I)、窒素(N)、酸素(O)といったさまざまな官能基をフェノール誘導体に導入することができます(図3右)。
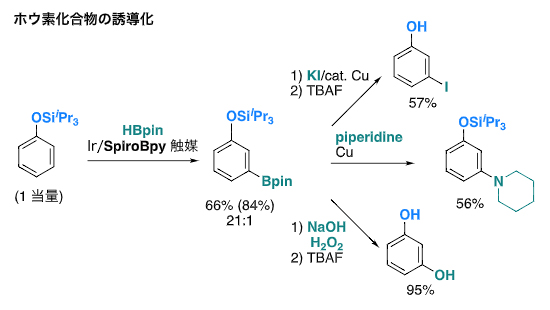
図3 ケイ素置換基で保護されたフェノール誘導体のメタ位官能基化の例
Ir/SpiroBpy触媒を用いて、ケイ素置換基(トリイソプロピルシリル基)で保護されたフェノール誘導体に、Bpin基(ピナコールボリル基)を導入するホウ素化反応を行うと、21:1の高いメタ位選択性で生成物が得られる。その生成物は既知の方法により、ヨウ素(I)、窒素(N)、酸素(O)といったさまざまな官能基を持つフェノール誘導体に変換できる。
一般に、フェノール誘導体の官能基化において、求電子的官能基化[9]ではオルト体とパラ体の混合物が、遷移金属触媒による炭素-水素結合官能基化ではメタ体とパラ体の混合物が生じるため、メタ体生成物のみを選択的に得る手法はこれまでありませんでした。本手法は、1工程でメタ体生成物を得られることから、単純でありながら難しかった古典的課題に対する直接的な解決法といえます。
今後の期待
ルーフ配位子を用いて有機化合物の遠隔位を立体制御するというコンセプトは、標的分子に合わせたさらなる配位子設計により、メタ位以外の炭素-水素結合の選択的な官能基化や、イリジウム以外の地球上に豊富に存在するさまざまな金属触媒を用いた選択的合成反応へ応用できる可能性を秘めています。
また、遷移金属触媒反応においてビピリジンが重要な役割を果たしている現状を考慮すると、3次元的なスピロビピリジン骨格を利用し、ルーフ部位に立体制御以外の機能を持たせた配位子を設計することで、新しい反応性や選択性を示す有用な反応の開発が期待できます。
さらに今回の研究は、国際連合が2016年に定めた17項目の「持続可能な開発目標(SDGs)[10]」のうち「12.つくる責任つかう責任」に大きく貢献する成果です。
補足説明
1.配位子
錯体化合物の中心金属原子に配位して、その性質を変化させたり機能を付与したりする化合物。
2.イリジウム(Ir)
周期表の第9族に属する原子番号77の遷移金属元素。芳香族炭化水素のホウ素化反応の触媒として最もよく用いられる金属の一つ。
3.触媒
化学反応の反応速度を速める物質。触媒自身は反応前後で変化しない。
4.芳香族炭化水素
炭素原子と水素原子からなる化合物のうち、ベンゼン環を含み芳香族性を示すもの。アレーンとも呼ばれる。
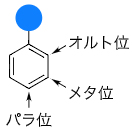
5.オルト位、メタ位、パラ位
一置換ベンゼンには、置換基(青丸)が結合した炭素原子以外に3種類の炭素がある。近い順にオルト位、メタ位、パラ位と区別される。
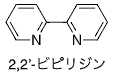
6.2,2′-ビピリジン
ピリジン分子が二つ炭素-炭素単結合でつながった分子をビピリジンという。金属の配位子としては、下に示す2,2′-ビピリジンがよく用いられる。
7.ホウ素化反応
置換反応や付加反応によりホウ素原子を導入する反応。本研究では、炭素に結合した水素原子をホウ素原子で置換している。
8.鍵と鍵穴モデル
ある酵素は特定の基質に対してのみ触媒作用を示す。このとき、基質と酵素の活性部位はそれぞれ、鍵と鍵穴の関係に例えられる。
9.求電子的官能基化
電子不足な性質を持つ求電子剤を用いる官能基化。ベンゼン環は電子豊富でそのπ電子が求電子剤との反応性に富むため、芳香族求電子置換反応が進行する。
10.持続可能な開発目標(SDGs)
2015年9月の国連サミットで採択された「持続可能な開発のための2030アジェンダ」にて記載された2016年から2030年までの国際目標。持続可能な世界を実現するための17のゴール、169のターゲットから構成され、発展途上国のみならず、先進国自身が取り組むユニバーサル(普遍的)なものであり、日本としても積極的に取り組んでいる(外務省ホームページから一部改変して転載)。
研究チーム
理化学研究所 環境資源科学研究センター 機能有機合成化学研究チーム
チームリーダー イリエシュ・ラウレアン(ILIES Laurean)
上級研究員 浅子 壮美(あさこ そうび)
特別研究員 ラマドス・ブーバラン(RAMADOSS Boobalan)
特別研究員 金 玉樹(きん ぎょくき)
研究支援
本研究は、日本学術振興会(JSPS)科学研究費補助金新学術領域研究(研究領域提案型)「Hybrid Metal Catalysis for C-H Functionalization of Simple Arenes(研究代表者:イリエシュ・ラウレアン)」、理化学研究所奨励課題(研究代表者:浅子壮美)、および創発物性科学研究センター物質評価支援チームによる支援を受けて行われました。
原論文情報
Boobalan Ramadoss, Yushu Jin, Sobi Asako, Laurean Ilies, “Remote steric control for undirected meta-selective C-H activation of arenes”, Science, 10.1126/science.abm7599
発表者
理化学研究所
環境資源科学研究センター 機能有機合成化学研究チーム
チームリーダー イリエシュ・ラウレアン(ILIES Laurean)
上級研究員 浅子 壮美(あさこ そうび)
報道担当
理化学研究所 広報室 報道担当