2020-11-27 量子科学技術研究開発機構
発表のポイント
- 分子内を歩き回る水素原子の時間分解計測により、分子内で起こる化学反応の新しいルートである「ローミング過程」の可視化に世界で初めて成功
- 従来の予測より5桁も速く進行する脱励起過程を発見
- 燃焼反応における化学組成の予測精度向上や新奇な化学反応の開拓につながる成果
国立研究開発法人量子科学技術研究開発機構(理事長 平野俊夫、以下「量研」という。)量子ビーム科学部門関西光科学研究所の遠藤友随研究員、国立大学法人東海国立大学機構名古屋大学(総長 松尾清一、以下「名古屋大学」という。)物質科学国際研究センターおよび同大学大学院理学研究科の菱川明栄教授ら、Institut national de la recherche scientifique, Centre Énergie, Matériaux et Télécommunications(INRS-ÉMT, カナダ)のFrançois Légaré教授、Heide Ibrahim博士らの国際共同研究グループは、分子内を歩き回る水素原子の姿を直接捉え、化学反応の新しいルートとして注目されているローミング過程を可視化することに世界で初めて成功しました。
1つの分子が2つ以上の断片に分かれる「解離反応」は、最もシンプルな化学反応の一つです。一般に化学反応は反応物と生成物の間にあるエネルギー障壁 1 ) を超えることで進みます。1920年代に量子力学の基礎となるシュレーディンガー方程式 2 ) が定式化されて以来、化学反応はエネルギー障壁が最も低いルートを経て速やかに進行する、という考えが定説となっています。ところが、防腐剤等の材料としてよく知られているホルムアルデヒド分子(H2CO)を対象に、障壁が最も低いルートを通らない新しい反応ルートの存在が2004年に予測されました。この反応では、ホルムアルデヒド分子中を水素原子(H)が歩き回り、別の水素原子と結合することで、最終的に水素分子(H2)と一酸化炭素分子(CO)に解離します。この過程は、水素原子が分子内を歩き回る様子(roaming)から「ローミング過程」と呼ばれ、これまでの化学反応とは異なる特徴を持った新しい分子内反応として注目されています。今回、本国際共同研究グループは、INRS-ÉMTと名古屋大学で、フェムト秒レーザー 3 ) を利用してホルムアルデヒド分子の解離反応の時間分解計測を行い、ローミング過程の可視化に世界で初めて成功しました。得られた実験結果は、量研、コーネル大学、エモリー大学、National Research Council of Canadaが共同で実施した量子力学に基づいた理論計算と比較・検証することでローミング過程に由来することを確認しました。さらに、ローミング過程の前段階として起こる脱励起過程が、従来予測された時間の10万分の1の極短時間で進行することを発見しました。これらの成果は、化学反応を分子形状の変化や電子の運動エネルギーの変化として観測することで、これまで隠れていた化学反応の詳細を明らかとしたものです。
今後は、本成果を基に、ローミング過程の全容を解明することで、燃焼反応中の化学組成の予測精度向上や従来の常識にとらわれない化学の実現が期待されます。例えば、ローミング過程の寄与が指摘されている、二酸化炭素から酸素が直接生成する解離反応の探究を進めることにより、火星や金星など二酸化炭素が豊富な環境下での酸素生成法等の新奇な化学反応の開拓につながる可能性も議論されています。
本研究成果はアメリカ科学振興協会(AAAS)が発刊する科学雑誌『Science』(T. Endo et al.)に2020年11月27日(金)4:00(日本時間)に掲載されます。
研究の背景
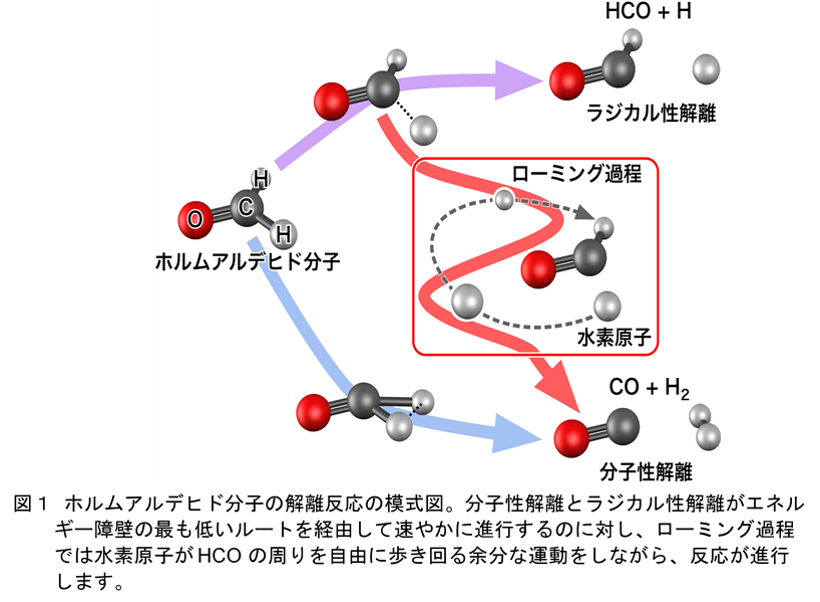
化学反応がどのようなルートを通って進むかを理解することは、反応の予測や新奇な反応の探索をする上で極めて重要です。1920年代に量子力学の基礎となるシュレーディンガー方程式が定式化されて以来、化学反応は反応物と生成物の間で最もエネルギーの低い(安定な)分子構造を経由して速やかに進行すると考えられてきました。例えば、図1に示したホルムアルデヒド分子(H2CO)の解離反応では、水素分子(H2)と一酸化炭素分子(CO)に解離する分子性解離(図1下、青矢印)と水素原子(H)とHCOに解離するラジカル性解離(図1上、紫矢印)という2つの反応ルートがよく知られています。これに対して、H2COを構成している1つの水素原子(H)が残りのHCOから一度遠くに離れたあと、もう1つの水素原子と結合して水素分子(H2)と一酸化炭素分子(CO)に解離する、新しい反応ルート(図1中、赤矢印)が実験・理論の両面から予測されました。2004年に提案されたこの反応ルートは、水素原子が分子内を自由に歩き回る様子(roaming)から「ローミング過程」と呼ばれています。ローミング過程はそれまでの化学反応の常識から外れたものでしたが、近年では、アルコール類や窒素酸化物など多くの分子の解離反応にも存在する普遍的な反応ルートであると考えられており、合成化学や大気化学の観点からも注目を集めています。
化学反応のルートをより深く理解するためには、時々刻々と変化する分子の姿を直接可視化する方法が必要です。非常に短い時間幅を持つレーザーを用いた超高速分光法 4) は、化学反応を原子や分子が運動する時間スケールで捉え、理解するための極めて強力な手法です。しかし、これまでにローミング過程で分子内を自由に歩き回る原子の姿を実際に捉えた例はありませんでした。これは、従来の手法は足並みの揃った運動による分子形状の変化を観測対象としており、反応開始のタイミングが個々の分子によって大きく異なるローミング過程のように、バラバラに運動する分子の姿を可視化することは困難なためです。今回、解離反応の進行に伴って時々刻々と変化するホルムアルデヒド分子の形状を超高速分光法の1つであるクーロン爆発イメージング法により時間分解計測し、量子力学に基づいた理論計算をおこなうことで、世界で初めてローミング過程を可視化することに成功しました。
研究手法と成果
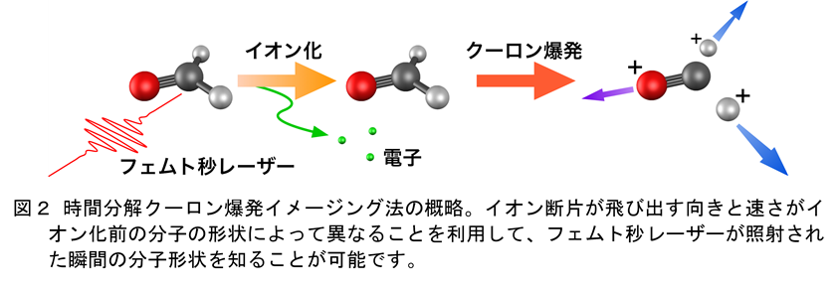
今回用いたクーロン爆発イメージング法の概略を図2に示しました。クーロン爆発イメージング法では、分子の振動周期と同程度のフェムト秒(1000兆分の1秒)という極めて短い時間幅を持つレーザー光を分子に照射し、瞬間的に複数の電子をはぎ取ることで分子をイオン化します。イオン化された分子は正電荷を帯びるため、電気的な反発(クーロン反発)により複数のイオン断片に分解します(クーロン爆発)。このときのイオン断片が飛び出す向き・速さを精密に測定すると、イオン化前の分子の形状を知ることができます。これは打ち上げられた花火の色と形が、打ち上げられる前の花火玉の中の火薬の種類と配置によって決まることに似ています。
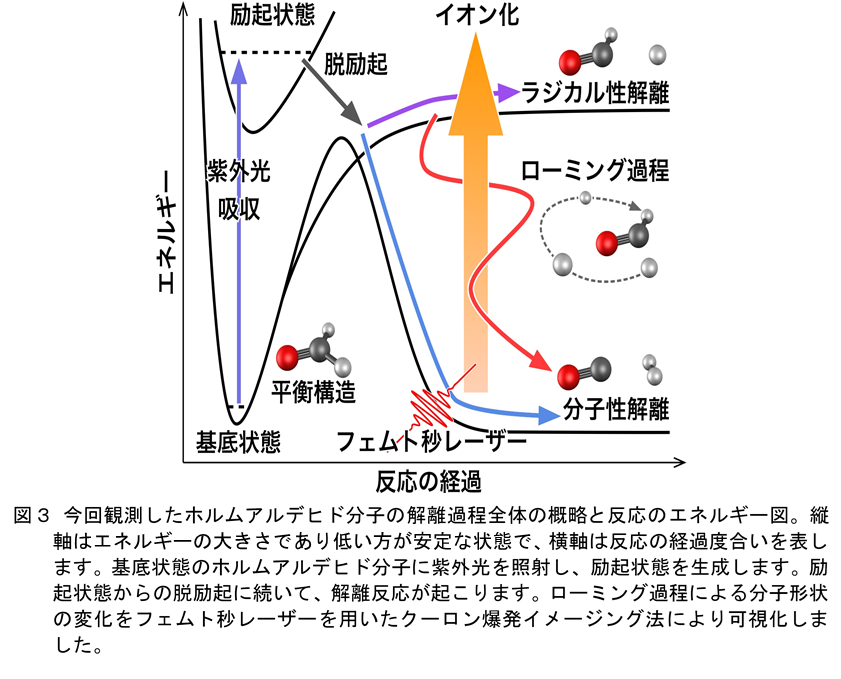
今回観測したホルムアルデヒド分子の解離反応の概略と反応のエネルギー図 5) を図3に示しました。まず、エネルギーが低い安定な状態(基底状態) 6) のホルムアルデヒド分子に紫外線領域の光を照射することで、エネルギーの高い不安定な状態(励起状態)6) のホルムアルデヒド分子を生成しました。不安定な状態の分子は余剰なエネルギーを放出し、よりエネルギーの低い安定な基底状態に戻ります(脱励起)。ホルムアルデヒド分子の場合には、この脱励起過程の後に解離反応が進行します。解離反応により時々刻々と変化する分子形状を観測するため、別のフェムト秒レーザーを照射し、ホルムアルデヒド分子を瞬間的にイオン化しました。イオン化に続いて起こるクーロン爆発によって分子から飛び出したイオン断片の向き・速さを精密に測定することでホルムアルデヒド分子の解離反応を可視化しました。
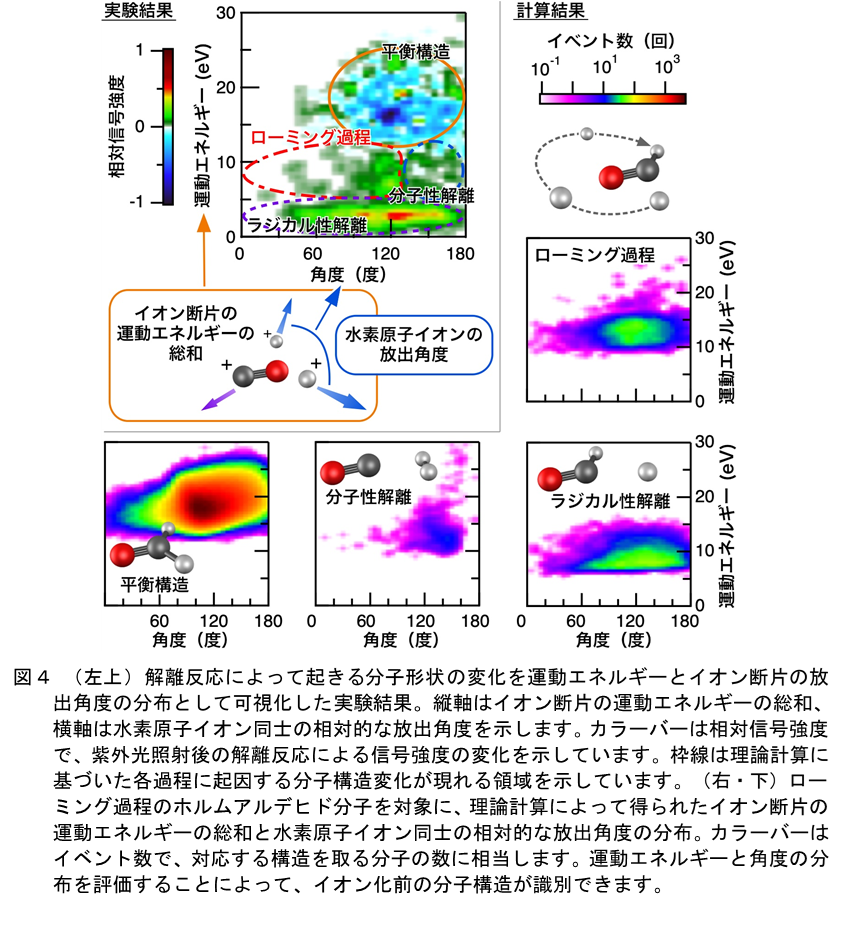
紫外光の照射後にフェムト秒レーザーを照射して得られた結果を図4(左上)に示しました。縦軸は1つの分子から飛び出した各イオン断片の持つ運動エネルギーの総和であり、エネルギーが高いほど原子間の平均的な距離が小さく、クーロン反発力が大きいことに対応します。また、横軸は2つの水素原子イオン同士の相対的な放出角度であり、イオン化前のホルムアルデヒド分子内での水素原子同士の相対的な位置関係を反映します。紫外光を照射することによる反応が起きていない平衡構造のままの分子(図4、橙色枠)が減少すると同時に、運動エネルギーの小さい(縦軸12 eV 7) 以下)領域(図4、赤・青・紫色枠)で信号が増加する様子が見られ、解離反応が進行していることが分かりました。今回、ローミング過程における分子構造の変化とイオン断片が飛び出す向き・速さの関係を精密に評価するため、ホルムアルデヒド分子の解離反応およびクーロン爆発過程に関して量子力学に基づいた理論計算を行いました。理論計算によって得られた分布(図4右および下)は実験結果を非常に良く再現しており、ホルムアルデヒド分子のローミング過程に由来することが確かめられました。
さらに、今回、脱励起過程についても従来の予測に反する結果が得られました。これまで紫外光吸収後に、ホルムアルデヒド分子が励起状態から基底状態に戻る(脱励起過程)には数十ナノ秒(10億分の1秒)程度の時間が必要であると予測されていました。今回、イオン断片の計測に加えて分子の状態をより直接的に調べられる光電子計測を行った結果、従来の予測より5桁も速い300フェムト秒でホルムアルデヒド分子が脱励起する様子の観測に成功しました。これは、時間分解計測をおこなうことで初めて発見された新しい脱励起過程です。
今回、クーロン爆発イメージング実験をInstitut national de la recherche scientifique, Centre Énergie, Matériaux et Télécommunications(INRS-EMT, カナダ)のAdvanced Laser Light Source(Director Prof. François Légaré)で、光電子計測実験を名古屋大学の光物理化学研究室(菱川明栄教授)で実施しました。それらの計測結果を元に、量研の超高速計測の解析技術や量研、コーネル大学、エモリー大学、National Research Council of Canadaの理論計算技術を組み合わせることで、ローミング過程の可視化へと繋がりました。近年、ローミング過程はホルムアルデヒド分子に限らず存在する普遍的な反応ルートであると考えられるようになり、その全貌解明に向けて、より詳細な情報が得られる超高速分光法を用いたローミング過程の直接観測が待ち望まれていました。今回、超高速分光法の1つである時間分解クーロン爆発イメージング法と量子力学を基盤とした理論計算を組み合わせることで、ホルムアルデヒド分子内を自由に歩き回る水素原子の姿を捉え、ローミング過程を可視化することに世界で初めて成功しました。また、従来の分光学的実験手法や理論計算での予測より5桁も速い脱励起過程を発見することにも成功しました。
本研究のインパクト
本成果は、これまで理論予測や間接的な観測にとどまっていた新しい化学反応ルート「ローミング過程」を、分子構造の変化として可視化し、その存在を実証したものです。また、本成果は、今回用いた研究手法が、これまでの中心的な研究対象であった光照射後に足並みを揃えて進む化学反応だけでなく、ローミング過程のように個々の分子で反応の開始するタイミングが大きく異なる化学反応の観測にも有効であることを示すもので、これまで隠されていた化学反応の全貌を明らかとする計測技術としての展開が期待されます。今後、ローミング過程の全容解明や、その寄与を取り入れたシミュレーションにより、身近な燃焼反応から宇宙空間における星間分子雲まで、幅広く行われている化学組成予測の精度向上につながることが期待できます。また、二酸化炭素から酸素が直接生成する反応でもローミング過程の寄与が予測されており、その詳細が解明されることで火星や金星など二酸化炭素が豊富な環境下での酸素生成法等の新奇な化学反応の開拓につながる可能性も議論されています。
用語解説
1) エネルギー障壁
化学反応が進行するために越えなければならないエネルギーの壁。分子はその中に含まれる原子の相対的な位置関係(分子構造)によりエネルギー(安定性)が変化します。化学反応が進行する、すなわち反応物から生成物へと分子の形状が変化するためには、エネルギーの高い分子構造(遷移状態)を経由する必要があります。
2) シュレーディンガー方程式
量子力学に従う電子や原子核の運動を記述するための方程式。
3) フェムト秒レーザー
フェムト秒(1000兆分の1秒)という極めて短い時間だけ光るレーザー光。
4) 超高速分光法
分子が振動するのに必要な時間よりも短い時間幅のレーザー光を利用して、ある瞬間の分子の構造や特性などを測定・評価する手法。代表的なものが、分子運動を開始するポンプ光と分子運動を観測するプローブ光を用いたポンプ-プローブ分光法です。
5) エネルギー図
反応の経過に伴う分子構造や分子の状態(電子状態・振動状態等)の変化とエネルギー変化の対応関係を表した図。
6) 基底状態と励起状態
通常、分子はエネルギーの最も低い基底状態として存在しています。光吸収などによって分子がエネルギーを受け取ると、エネルギーの高い励起状態に変化します。一般に励起状態は基底状態よりも不安定であり、励起状態の分子では解離反応が進行したり、余剰なエネルギーを放出することで基底状態に戻ったりするなどの現象が起こります。
7) eV(電子ボルト)
エネルギーの単位の1つ。1 eVは電子が1 Vの電位差で加速された時に得るエネルギーに相当します。