2022-05-02 アメリカ合衆国・イリノイ大学アーバナ・シャンペーン校
・ イリノイ大学アーバナ・シャンペーン校 化学・バイオ分子工学部(ChBE)と米国エネルギー省(DOE)のバイオエネルギー研究センター (BRC)の Center for Advanced Bioenergy and Bioproducts Innovation(CABBI)が、新酵素による新生体触媒反応を通じて有用な化学物質を生成する技術を開発。
・ 自然界には見られない反応現象を起こす酵素を作ることができれば、植物ベース油脂のバイオ化学品へのアップグレード等で、合成化学における積年の課題の解決に貢献できる。
・ 有機体でタンパク質分子の酵素が化学反応を触媒する生体触媒反応は、環境負荷が低く、比較的安価でエネルギー消費量の少ない極めてサステナブルなプロセス。有機溶媒や熱等を要する化学触媒とは対照的な、生体触媒反応現象を利用した化学物質の合成が注目されている。
・ 過去の研究において、酵素 ene-reductase(ER)を生体触媒として使った可視光が誘発する反応で、高価値化学物質の製造に利用できる対掌性のカルボニル化合物の高収率生成に成功している。
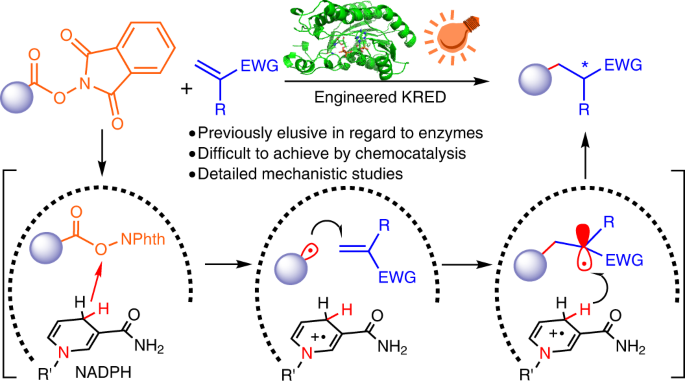
・ この成果を踏まえ、本研究では可視光による光生体触媒反応を通じた新しい酵素反応の創出に着目。微生物が生産するニコチンアミド依存性ケトレダクターゼを使用し、化学触媒では極めて困難な、自然界にはない新しい生体触媒反応メカニズム(非対称性ラジカル共役付加反応)でα-キラルエステルを生成した。
・ 今回の成果は、ソルガムやエナジーケーン等の植物からバイオ燃料やバイオケミカルを製造するCABBI の研究活動に実用的なアプリケーションを提供するもの。これらの植物の脂肪酸を出発原料として使用した石鹸やスキンケア製品の原料のような、高付加価値のバイオ製品の環境に優しい合成が可能となる。
・ CABBI の(植物から高価値化学物質への変換)研究活動や、一般的なバイオエネルギー研究における大きな変化の一つには、目的の燃料や化学物質を合成する望ましい働きと基質特異性を備えた酵素の不足がある。このような酵素を発見・創出する新手法の開発を急ぐ必要がある。
URL: https://cabbi.bio/researchers-develop-powerful-strategy-for-creating-new-to-nature-enzymes/
<NEDO海外技術情報より>
関連情報
Nature Catalysis 掲載論文(アブストラクトのみ:全文は有料)
Photoinduced chemomimetic biocatalysis for enantioselective intermolecular radical conjugate addition
URL: https://www.nature.com/articles/s41929-022-00777-4
Abstract
Exploiting nature’s catalysts for non-natural transformations that are inaccessible to chemocatalysis is highly desirable but challenging. On the one hand, the widespread nicotinamide-dependent oxidoreductases have not been utilized for single-electron-transfer-induced bimolecular cross-couplings; on the other, the addition of catalytic asymmetric radical conjugate to terminal alkenes remains a challenge owing to strong racemic background reaction and unselective termination of prochiral radical species. Here we report a chemomimetic biocatalysitic approach for construction of alpha-carbonyl stereocentres via an unnatural intermolecular conjugate addition of N-(acyloxy)phthalimides-derived radicals with acceptor-substituted terminal alkenes, by combination of visible-light excitation and nicotinamide-dependent ketoreductases (KREDs). Based on protein crystal structure, we engineered KREDs via a semi-rational mutagenesis strategy to improve reaction outcomes with a small and high-quality variants library. Mechanistic investigations combining wet experiments, crystallographic studies and computational simulations demonstrate that the repurposed biocatalyst can suppress racemic background reaction and unselected side reactions, yielding enantioselectivity that is challenging to achieve by chemocatalysis.


