医学と生命科学の発展に幅広く貢献
2020-05-12 量子科学技術研究開発機構
発表のポイント
- ナノサイズの特殊なダイヤモンドセンサーを用いて、生きた細胞内にある生体分子が起こすナノスケールの回転運動を3次元で計測する新たな技術を開発した。
- 位置変化を伴わない生体分子の回転運動として、ATPaseがATPを合成するときの回転運動や抗がん剤がターゲットとなるがん細胞表面の受容体に結合したときの動きの変化を計測することに成功した。
- 世界最小の3次元回転センサーとして、新薬研究や再生医療の幹細胞モニタリングなど、生命科学の新たな計測ツールとして幅広い活用が期待できる。
発表概要
国立研究開発法人量子科学技術研究開発機構(理事長 平野俊夫。以下「量研」という。)量子生命科学領域 次世代量子センサーグループの五十嵐龍治グループリーダーは、広島大学の杉拓磨特任准教授、大阪大学蛋白質研究所の原田慶恵教授、量研 量子生命科学領域の白川昌宏領域研究統括(京都大学教授)らと共同で、大きさが1万分の1ミリメートル以下のナノサイズの特殊なダイヤモンドをセンサーとして用い、1分子のたんぱく質が回転する動きを捉えることに成功しました。
NVセンター1)と呼ばれる原子配列の乱れを含むダイヤモンドは、生命現象を精密計測する「ナノ量子センサー2)」として注目されています。研究グループはこのセンサーが磁気センサーであるという特徴を巧みに利用し、3次元回転センサー3)として利用する新たな技術を開発しました。この技術を用い、これまで顕微鏡では捉えることのできなかった生きた細胞における生体分子の回転運動、例えばATP4)合成・分解酵素(ATPアーゼ)の回転運動やがん細胞表面の分子が抗がん剤と結合して回転運動に変化が生じる現象を計測することに成功しました。
この技術は、従来捉えられなかった生体分子の位置変化を伴わないわずかな回転運動を観察できるため、生命科学における新たな計測ツールや、薬剤標的たんぱく質の運動を指標とした医薬品のスクリーニング技術として利用されることが期待されます。
この研究成果は化学分野において最も権威のある雑誌の一つである米国化学会発行の「Journal of the American Chemical Society」のオンライン版に2020年4月14日(火)(米国時間)に掲載されるとともに、掲載当月の評価が特に高い研究内容としてSpotlightsで紹介およびSupplementary Journal Coverに採択されました。
本研究は、JST 戦略的創造研究推進事業 さきがけ「コンポジット量子センサーの創成 -1細胞から1個体まで」(JPMJPR18G1)、さきがけ「ナノダイヤモンドによる三次元構造動態イメージング技術の創成」(JPMJPR14F1)および文部科学省 光・量子飛躍フラッグシッププログラム(Q-LEAP, JPMXS0118067395)の支援を受けています。また、MEXT/JSPS科研費 (JP18K19297, JP26220602, JP26286028, JP18H01838, JP15H05931, JP18H05474, JP18J10796, JP19H05380, JP19K16089)、JST戦略的創造研究推進事業CREST(JPMJCR1333)、最先端・次世代研究開発支援プログラム(LS072)、日本医療研究開発機構革新的先端研究開発支援事業PRIME(19gm6110022h001)の支援も受けています。
研究の背景
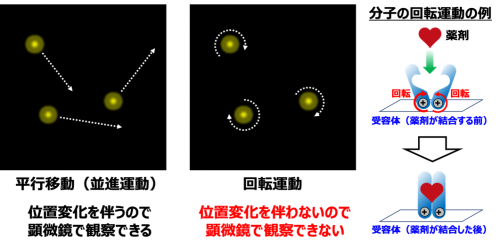
近年、センサーはとても身近なものになってきています。例えば、カメラの手ブレ補正や自動運転車なども、超小型の回転センサーの登場で実現しました。もし細胞内で使えるほど小さな回転センサーが開発されたならば、細胞や分子の微妙な運動変化を敏感に捉えることができるようになり、生命における多くの謎の解明につながります。 これまで2014年にノーベル化学賞を受賞した超解像蛍光顕微鏡が開発されたことで、位置変化を伴う生体分子の平行移動(並進運動)については、微細な動きを捉えられるようになりました。しかし、回転方向の運動は一般に位置変化を伴わないため、高性能な超解像蛍光顕微鏡を使っても観察することはできません(図1)。近年になって分子レベルの回転を検出するいくつかの方法が考案されましたが、それでもなお立体的な回転運動を三次元的に観察することは不可能でした。
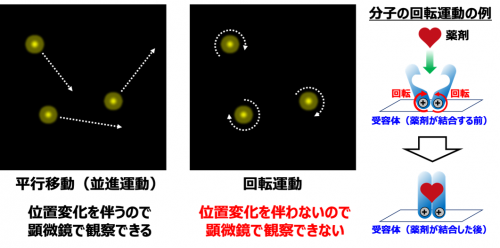
図1 平行移動(並進運動)と回転運動。一般に小さい分子の回転運動は位置変化を伴わないため顕微鏡で観察することはできません。もし分子の回転運動を詳細に観察できるようになれば、薬剤の効果なども効率よく解析できるようになる可能性があります。
開発した技術と成果
研究グループは、ナノサイズ(1ナノメートルは1ミリメートルの100万分の1)のダイヤモンド(ナノダイヤモンド5))が持つナノ量子センサーとしての働きに着目しました。このセンサーはダイヤモンド結晶中に「NVセンター」と呼ばれる電子を含んだ格子欠陥があり、そこから発する蛍光の情報を解析することで、さまざまな情報を得ることができる極めて小さなセンサーです。そのサイズは100ナノメートル以下であり、細胞内や細胞内小器官の磁場、温度、電場、pHなどを計測できる技術を開発してきました。
今回、研究グループは、このナノダイヤモンドが優れた磁気センサーであるという特徴を巧みに利用し、3次元回転センサーとして利用する新たな技術を開発しました。ナノダイヤモンドが持つNVセンター中の電子には磁石としての性質があります。電子はわずかな磁場でも影響を受けて、NVセンターから発する蛍光の強さを変化させます。そこで、まず外部から一方向の磁場をかけ、NVセンターが受ける磁場の向き、すなわち蛍光強度の変化量を計測し、磁場の向きを基準として、ナノダイヤモンド中のNVセンターの電子の向きが何度傾いたかを精密に決定できる技術を開発しました。さらに、異なる向きから複数の磁場をかけて同様に計測することで、ナノダイヤモンドが3次元で回転運動を観察できる回転センサーとして働くことを見いだしました(図2)。
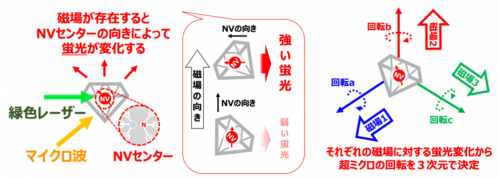
図2 ナノ量子センサーを用いた超ミクロ回転の3次元観察法。NVセンターは緑色のレーザーを受けると赤い蛍光を発する。この赤い蛍光はマイクロ波照射によって蛍光の減弱が起こるが、NVセンターの向きによって減弱の度合いが変わるので、蛍光の強さからNVセンターの向き(つまりダイヤモンドの向き)がわかる。そのため様々な磁場を与えながら蛍光測定を行うと、NVセンターの方向や回転運動を3次元で決定できる。
本研究で開発した技術を検証する実験として、ATPアーゼと呼ばれる酵素の回転運動を計測しました。ATPアーゼは生物の細胞の中で、エネルギー貯蔵のためのATP合成や、ATPの分解エネルギーを利用した水素イオンの輸送などを担っています。またこの酵素は、ATPを分解するときに中央にある軸部分のたんぱく質(γサブユニット)を回転させることから「地上最小のモーター」ともいわれています。そこで、ほぼ全ての生物に共通なATPアーゼであるF1-ATPaseを対象として、このγサブユニットにナノダイヤモンドを連結し、ATPを加水分解する際に起こるモーターの回転運動を計測しました。その結果、γサブユニット1分子の回転運動を3次元で観察することに世界で初めて成功しました(図3)。
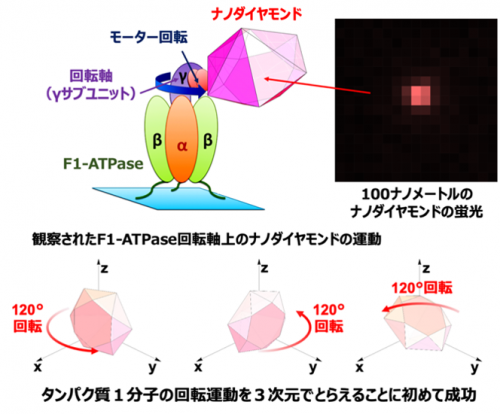
図3 ナノ量子センサーによるF1-ATPaseのモーター回転運動の1分子3次元観察。(上左)F1-ATPaseにナノダイヤモンドを結合させたものの模式図。(上右)F1-ATPaseに結合したナノダイヤモンドからの蛍光の写真。(下)F1-ATPaseに結合したナノダイヤモンドは、120°の回転を1単位とする運動を繰り返す。この運動を3次元的に観察することに成功した。(下段は実測データに基づいて再構成したもの)
またこの技術を利用して、細胞表面にある生体分子の運動が薬剤で変化する様子を計測しました。上皮成長因子受容体(EGFR)6)と呼ばれるたんぱく質は、上皮がん細胞上に多く存在することが知られており、がんを治療する薬剤の標的分子として注目されています。この分子にナノダイヤモンドを連結しておくことで、上皮がん細胞の一種であるA431細胞7)上のEGFR が抗がん物質(ラトランクリンA)の標的としてどのような影響を受けるかを、ナノダイヤモンドの動きを指標として計測したところ、抗がん剤が結合することでEGFRの回転運動に変化が生じる現象を新たに見いだしました(図4)。この手法は、創薬研究において、がん細胞上の標的分子に結合できる薬剤を効率的に探すためのツールとして活用が期待できます。
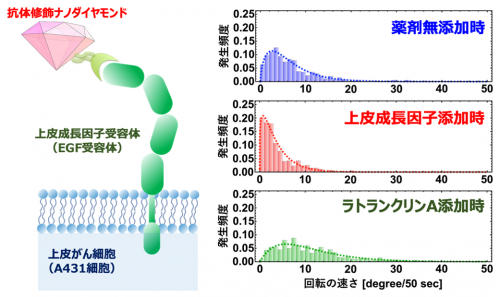
図4 上皮がん由来の細胞(A431細胞)に対する抗がん物質(ラトランクリンA)の影響。A431細胞上に多く発現する上皮成長因子受容体(EGF受容体)を抗体修飾ナノダイヤモンドで標識し3次元回転を観察。ラトランクリンAの添加による回転の促進が1細胞レベルで観察され、ラトランクリンAの抗がん作用による細胞膜上の運動の促進が確認できた。
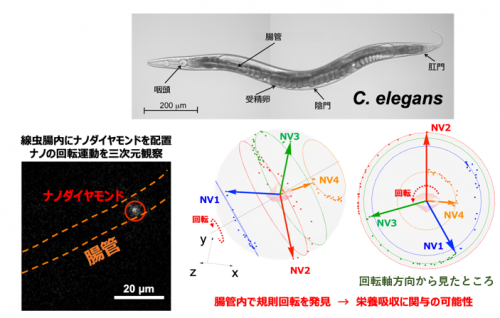
他にも、線虫C. エレガンス8)と呼ばれる体長1ミリメートル程度の微小生物において、栄養吸収を担う腸管腔で餌となる大腸菌の様な微粒子がどのように運動するかを観察するため、大腸菌と一緒にナノダイヤモンドを食べさせました。その結果、当初の予想ではC. エレガンスの腸内でランダムな動きをすると考えられたナノダイヤモンドが規則的な回転運動を示すことを見いだしました(図5)。C. エレガンスは老化のモデル生物として研究が進んでおり、腸内運動は栄養吸収効率と関係していることから、今後、この技術が老化のメカニズム解明にも寄与するのではないかと期待しています。
図5 C. エレガンス腸管内において発見した規則的な超ミクロ回転運動。(上)C. エレガンスの全身の写真。(下左)C. エレガンス腸内のナノダイヤモンドの写真。(下右)ナノダイヤモンド内の4つのNVセンター(NV1~NV4)の軌跡(各色の点)は、単純な回転運動をしており、このナノダイヤモンドが規則的な回転運動を行っていることを示している。
今後の展開
本研究では、従来計測が困難であった生きた細胞における生体分子の微細な3次元の回転運動について、ナノダイヤモンドNVセンターの性質を利用したナノ量子センサーで計測する技術を確立しました。このセンサーは極めて小さなサイズであり、1個の細胞の中にある1個の生体分子の計測が可能です。生命現象を担うたんぱく質やDNAなどの微細な分子の動きを捉えることは非常に難しく、その多くは顕微鏡では観察できません。この技術によって、生きた細胞の中で生体分子の微細な動きをリアルタイムで詳細に捉えられるようになれば、生命における多くの謎の解明につながります。また、薬剤が標的となるたんぱく質と結合すると、標的たんぱく質は構造変化を起こし、部分的に回転運動に微小な変化を生じることが知られています。従って、その回転運動に影響を及ぼすことができる薬剤の開発・探索は創薬研究に新しい視点を提供するものであり、ナノ量子センサーによる計測技術が新薬探索ツールとして活用されることも期待されます。
また今回発表した論文では、細胞膜上のナノダイヤモンドの回転運動が細胞骨格の秩序と関係していることも明らかにしています。幹細胞9)の分化は細胞骨格の秩序と密接に関係していることが知られており、本技術は、再生医療における幹細胞の分化状態や生着10)性、異常化などを1細胞レベルで観察することにも利用できると考えています。
この様に大きな可能性を秘めるナノ量子センサーの開発を推し進めることで、認知症などの神経疾患、発がん、免疫機能発現や老化など細胞生理メカニズムの解明、更に新たな治療法の開発まで、医学と生命科学の発展に幅広く貢献しようとしています。
用語解説
1)NVセンター
ダイヤモンド結晶中の不純物窒素(Nitrogen)と、その隣に形成された空孔(Vacancy)が作る原子配列の乱れ・欠陥。NVセンターは周辺環境の変化に極めて敏感に検知して量子状態が変わる特性があり、この特性をセンサーとして利用できる。このため、NVセンターを持つダイヤモンドは「量子センサー」と呼ばれて注目されている。本研究のNVセンター作成は量研高崎量子応用研究所の電子照射施設において行われた。
2)ナノ量子センサー
量子力学の原理に基づいてさまざまな物理量を計測するための装置、機器、素子などのこと。高感度で磁気計測を行えることから、量子センサーを用いた脳磁図検査の高感度化や装置の小型化などへの応用が期待されている。
3)(3次元)回転センサー
モーションセンサーの一種で、ジャイロセンサーなど回転方向の動きを検知するセンサー。物体の3次元的な回転運動を正確に理解するためには、x軸、y軸、z軸など独立した3つの軸の周りをどのように回ったかを知る必要がある。これを実現するセンサーは3次元回転センサー(または3軸回転センサー)と呼ばれる。これまでナノ領域では2軸に対する回転計測が限界だったため、3次元的な回転運動を観察することはできなかった。
4)ATP
微生物、植物、動物を含むあらゆる細胞内に存在し、生命の維持に必要なエネルギーの貯蔵や利用、物質の代謝や合成などを担う小分子。アデノシン三リン酸。細胞内では一般にエネルギーを生産する場所と使用する場所が異なるため、生産されたエネルギーはいったんATPの形で使用する場所まで運ばれる。このためATPは「生体のエネルギー通貨」などとも形容される。
5)ナノダイヤモンド
おおよそ100ナノメートル以下のダイヤモンドをナノダイヤモンドと呼ぶ。研究や工業分野などでは人工的に作られたダイヤモンドが用いられる。化学構造は宝飾品として用いられる天然のダイヤモンドと全く同じだが、人工ナノダイヤモンドは非常に安価なため、研磨剤やエンジンオイルの添加剤、鉛筆の芯の潤滑剤などとしても幅広く利用されている。
6)上皮成長因子受容体(EGFR)
体内において細胞の成長を制御する上皮成長因子(EGF)を認識し、細胞の分化・増殖のシグナル伝達を担う受容体。臓器の発達や形成において重要役割を果たす。また、さまざまな悪性腫瘍でEGFRの過剰発現や遺伝子変異が見られ、がんの予後不良因子としても知られる。
7)A431細胞
ヒトの表皮がん由来の培養細胞株の一種で、異常高レベルのEGFRを発現するため、細胞周期やがん関連の細胞内シグナル伝達経路の研究に使用される。
8)線虫C. エレガンス
体長1ミリメートル程度の多細胞生物で、2002年ノーベル生理学・医学賞の「プログラム細胞死」(シドニー・ブレナー、ロバート・ホルビッツ、ジョン・サルストン)、2006年ノーベル賞生理学・医学賞受賞の「RNA干渉」(アンドリュー・ファイア、クレイグ・メロー)、2008年ノーベル化学賞受賞の「緑色蛍光たんぱく質」(マーティン・チャルフィ)にも用いられた優れたモデル生物として知られる。特に近年、C.エレガンスの栄養状態と寿命との密接な関係が明らかになり、老化研究の優れたモデル系として期待されている。
9)幹細胞
さまざまな細胞に分化する能力を持つ細胞で、体内の組織や器官の維持において細胞を供給する役割を持つ。また、ケガや病気などで失った身体機能を再生する再生医療において活用が進む。
10)生着
移植した細胞等が、本来機能する組織に移動・定着し、機能を果たすようになること。