2023-09-04 生命創成探究センター
自然科学研究機構 生命創成探究センター / 生理学研究所の石井宏和助教、大友康平准教授(順天堂大学大学院医学研究科 兼任)、Ching-Pu Chang研究員、根本知己教授は、北海道大学大学院医学研究院の渡辺雅彦教授、山崎美和子准教授、東北大学未来科学技術共同研究センターの横山弘之教授と共同で、全パルス光源・タイムゲート検出系を駆使した独自の超解像二光子顕微鏡の開発に成功しました。
本研究成果は、国際科学雑誌 「PLOS ONE」 (2023年8月24日付) に掲載されました。
全パルス光源・タイムゲート検出系を駆使した超解像二光子顕微鏡の開発
発表のポイント
- 全パルス光源・タイムゲート検出系を駆使した超解像二光子顕微鏡(全パルス式二光子STED顕微鏡)の開発に成功しました。
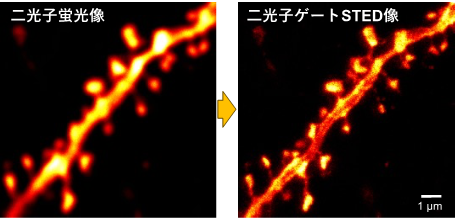
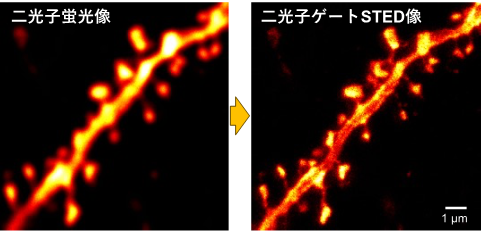
- 従来の超解像二光子像(二光子STED像)に比べてさらに約1. 4倍も高い空間分解能でマウス固定脳スライスにおけるスパインの微細形態を可視化することを可能にしました。
- 脳組織深部などで起こるナノスケールの生命現象の可視化を通じて、 生物学・医学研究の更なる発展に 貢献することが期待されます。
背景
二光子励起顕微鏡法*1は、生体内をありのままにサブミクロンの空間分解能で観察することを可能とし、医学・生物学研究の発展に大きく貢献しています。しかし、空間分解能については、対物レンズの開口数と二光子励起波長によって規定される励起光の回折広がりにより、300 nm程度でしかイメージングできないという大きな制約があります。そのため、二光子励起顕微鏡法は、三次元的な広がりを持つ神経回路網や、その回路網を伝搬する神経活動などを生体脳内で観察することを可能としてきましたが、記憶や学習によって変化する神経同士のつなぎめであるシナプス後部(樹状突起スパイン)の微細な形態変化を可視化するのは困難です。近年、この従来の可視化限界を打破し、100 nm以下の空間分解能(ナノスケール)で超解像イメージングするための方法論が盛んに提案されています。例えば、二光子励起顕微鏡法に、2014年のノーベル化学賞の受賞対象となった超解像技術 ”誘導放出制御(STED)*2 ”を融合させることが試みられています。最近、この二光子励起STED顕微鏡法を用いることで生体脳内のスパイン形態の時空間ダイナミクスをナノスケールで可視化したという報告がいくつかありましたが、高度で複雑な光源系・光学系を構築する必要があり、広く一般化された技術とは言い難い状況でした。
本研究の内容
我々は超解像技術の黎明期より独自の光技術を統合し、コンパクトかつ低侵襲的な超解像二光子励起STED顕微鏡の開発を進めてきました。その空間分解能は従来の二光子励起顕微鏡の約5倍、70 nmに達しましたが、脳組織スライスなど比較的厚みのあるサンプルでは、STED光照射に起因するバックグラウンドシグナルの上昇により空間分解能が顕著に劣化するといった問題がありました。本研究では、蛍光光子をサブナノ秒の精度でタイムゲート検出するためのシステムを新たに導入し、二光子励起はもちろんSTEDにもパルスレーザー光源*3を採用した二光子励起ゲートSTED顕微鏡(全パルス式二光子STED顕微鏡)を世界に先駆けて開発することに成功しました。1)全パルス光源系を用いることで観察対象への光照射を極限まで削ぎ落としSTED顕微鏡法でしばしば問題となる光ダメージの影響を抑えること、2)蛍光光子のタイムゲート検出*4により空間分解能の劣化に繋がる生体分子由来のバックグラウンドシグナルを除去すること、の両方を同時に実現することができました。特に脳組織イメージングにおけるタイムゲート検出の効果はこれまで考えられてきた以上に大きく、ゲート検出範囲の最適化により従来の二光子STED像に比べてさらに約1. 4倍も高い空間分解能でマウス固定脳スライスにおけるスパインの微細形態を可視化できることを見出しました(図1)。
本研究の意義と展望
本研究では世界ではじめて全パルス光源・タイムゲート検出系を駆使した超解像二光子励起顕微鏡を開発し、タイムゲート検出がこれまで考えられてきた以上に脳組織の二光子STED像の空間分解能の向上に寄与することを見出しました。また本システムは、従来の二光子励起顕微鏡の利点や操作性を損なうことなく、観察者が再現よく効率的にイメージングできることをコンセプトに構築された点にも意義があります(図2)。ただ実際の生体深部観察へと展開するには、組織による光学収差を補償する技術や、明るい蛍光プローブの選定・開発、多色化なども重要です。今後は、生きたまま、ありのままで、体の中を電子顕微鏡のように観察できる「生体ナノイメージング」を目指して、1つ1つの課題をクリアしていきたいと考えています。
なお、本研究で開発した全パルス式二光子STED顕微鏡は、自然科学研究機構 生命創成探究センターの共同利用機器として広く利用者を募っています。知る限り日本で二光子励起STED顕微鏡を開発・運用している研究機関は当センターのみであり、ナノイメージングを通じて生物学・医学研究の更なる発展を推し進める一役を担いたいと考えています。
(参考)生命創成探究センター 機器案内 超解像顕微鏡システム 2光子STED顕微鏡
研究サポート
本研究は、AMED革新脳プロジェクト(JP19dm0207078 根本知己)、科学研究費補助金 (JP15H05953 “Resonance Bio” 根本知己; JP16H06280 “Advanced Bioimaging Support” 根本知己; JP18K14659 石井宏和; JP20H00523 根本知己; JP20H05669 根本知己; JP21K19346 大友康平; JP22H02756 大友康平)、光科学技術研究振興財団研究助成 (石井宏和)、ExCELLS若手奨励研究 (石井宏和) 等の支援を受けて実施されました。
掲載論文
雑誌名: PLOS ONE
論文名: All-synchronized picosecond pulses and time-gated detection improve the spatial resolution of two-photon STED microscopy in brain tissue imaging
著者: Hirokazu Ishii, Kohei Otomo, Ching-Pu Chang, Miwako Yamasaki, Masahiko Watanabe, Hiroyuki Yokoyama, Tomomi Nemoto* (*責任著者)
DOI: 10.1371/journal.pone.0290550
掲載URL: https://doi.org/10.1371/journal.pone.0290550
用語説明
*1 二光子励起顕微鏡法
蛍光分子が、2つの光子を同時に吸収して励起状態に遷移する非線形光学現象を利用した蛍光顕微鏡法の一種。従来の蛍光顕微鏡法と比べてより深い領域を低侵襲的に観察できるといったメリットがある。
*2 誘導放出制御(STED)顕微鏡法
100年以上にわたって超えることができないと考えられていた蛍光顕微鏡の空間分解能の限界を打破した超解像技術の一種。励起光とは異なる波長の光(STED光)を高強度でサンプルに照射する必要があり、しばしばサンプルに対する光ダメージが問題になる。
*3 パルスレーザー光源
ある一定の間隔でレーザー光を周期的に発振する光源。本研究では、二光子励起とSTED用に独自に開発した2種類のパルスレーザー光源を使用しており、それぞれのパルスタイミングを10ピコ秒(1000億分の1秒)の精度で電気的に同期させている。
*4 タイムゲート検出
パルス光励起により放出された蛍光光子数の時間変化を計測し、特定の時間枠内の蛍光光子のみを検出する技術。
お問い合わせ先
研究に関するお問い合わせ
自然科学研究機構 生命創成探究センター / 生理学研究所
教授 根本 知己
広報に関するお問い合わせ
自然科学研究機構 生命創成探究センター 研究戦略室
自然科学研究機構 生理学研究所 研究力強化戦略室