2021-01-29 愛媛大学,科学技術振興機構
ポイント
- キラリティ検出のために波数軸に加えてさらに時間軸と空間軸を追加した多次元赤外円二色性システム(熱光源と量子カスケードレーザーの切り替え可能なコンカレントシステム)を開発しました。
- 水溶媒の影響を受けるアミドⅠ,Ⅱ領域において種々の試料形態に対応できる顕微技術の開発に成功しました。
- ジペプチドの固体状態においても高信頼性のシグナル検出ができるようになりました。アミドⅠ領域を始めとして、シグナルの増大を見いだし、アキラル部分のキラル誘導を確認しました。熱光源測定と比較して、測定時間も短縮できました。
- 自動ステージ機能により空間をスキャンさせる測定手法を開発し、サンプル内の異なる位置でのキラリティの違いを検出することも可能となりました。
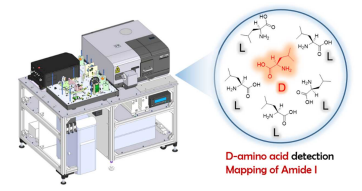
愛媛大学 大学院理工学研究科 佐藤 久子 教授の研究グループは、日本分光株式会社 小勝負 純 部長、横浜国立大学 大学院工学研究院 川村 出 准教授、北里大学 理学部 吉田 純 講師との共同で、量子カスケードレーザーを用いたスキャン機能型の多次元赤外円二色性分光装置の開発に成功しました。
アミノ酸は、同一の化学式であってもL体とD体という左右対称な立体化学のものが存在する、キラリティという性質を有しています。たんぱく質は、通常L体のアミノ酸(L-アミノ酸)が多数結合した生体高分子ですが、そのうちの1つがD体のアミノ酸(D-アミノ酸)に変異した場合に、それがたんぱく質の構造や性質に与える影響については、生物物理学、医学分野で非常に重要なテーマになっています。例えば、これはアルツハイマー病の原因物質であるアミロイド線維の生成メカニズムの解明にもつながっています。
佐藤教授らは、こうしたキラリティの解析を迅速かつ生体試料のままで行うためには新しい分光学的手段が必要との観点から、今回、「多次元赤外円二色性分光法」と呼ばれる測定装置を開発しました。従来型の装置では赤外波の波数に対してキラリティを測定していたものに、今回の装置ではさらに時間軸と空間軸を追加することに成功しました。
今後、この顕微スキャン技術を駆使して、従来手法では水溶媒の影響を受けて測定困難だったアミドⅠ,Ⅱ領域のシグナルを検出することで、種々の試料形態におけるキラリティ解析手法を確立することを目指しています。
本研究の成果は、アメリカ化学会(ACS)の「Analytical Chemistry」に2021年1月29日(日本時間)に掲載される予定です。
本研究は、JST 未来社会創造事業 探索加速型「共通基盤」領域の研究開発課題「多次元赤外円二色性分光法の開発」(研究開発代表者:佐藤 久子)(JPMJMI18GC)の支援を受けて行いました。
<論文タイトル>
- “Multidimensional Vibrational Circular Dichroism Apparatus Equipped with Quantum Cascade Laser and Its Use for Investigating Some Peptide Systems Containing D‑Amino Acids”
- DOI:10.1021/acs.analchem.0c02990
<お問い合わせ先>
<研究に関すること>
佐藤 久子(サトウ ヒサコ)
愛媛大学 大学院理工学研究科 教授
<JST事業に関すること>
水田 寿雄(ミズタ ヒサオ)
科学技術振興機構 未来創造研究開発推進部