2020-05-01 京都大学
萩野浩一 理学研究科教授、前野悦輝 同教授は、原子核の陽子の数に着目した、新しい周期表「ニュークリタッチ」を考案しました。
今回考案した周期表は、中学の教科書にも登場する元素の周期表に似ていますが、元素記号の並び方が異ななる「原子核」の周期表です。すい、へー、りー、ベー(水素(H)、へリウム(He)、リチウム(Li)、ベリリウム(Be))の順は同じですが、ヘリウムの下には希ガス安定元素のネオン、アルゴンなどではなく、酸素、カルシウムなどが並んでいます。
原子核に含まれる陽子の数が、魔法数(マジック・ナンバー)と呼ばれる2、8、20、28などになるとき原子核が安定になることは良く知られています。しかし、それを周期表の形にした例はこれまでありませんでした。
元素の周期表との比較が容易な原子核の周期表ができたことによって、魔法数を含めて原子核の性質を学ぶ上での新しい指標ができます。今後は大学の教科書などにもこの原子核の周期表が掲載され、教育に活用されることが期待されます。
本研究成果は、2020年4月21日に、国際学術誌「Foundations of Chemistry」のオンライン版に掲載されました。

図:今回考案した新しい原子核の周期表
詳しい研究内容について
―原⼦核の周期表「ニュークリタッチ」― 概要
まず下の新しい周期表をご覧ください。中学の教科書にも登場する元素の周期表に似ていますが、元素記号の並び⽅が異なります。すい・へー・りー・ベー(⽔素 H・へリウム He・リチウム Li・ベリリウム Be)の順は同じなのですが、ヘリウムの下には希ガス安定元素のネオン、アルゴンなどではなく、酸素、カルシウムなどが並んでいます。
実はこれは「原⼦核」の周期表です。原⼦核に含まれる陽⼦の数が、魔法数(マジック・ナンバー)と呼ばれる 2, 8, 20, 28…になるとき原⼦核が安定になることは良く知られています。しかし、意外なことにそれを周期表の形にした例はこれまで⾒当たりませんでした。この新しい周期表は、京都⼤学⼤学院理学研究科の萩野浩⼀・前野悦輝両教授が考案したものです。
この成果は、Springer Nature 社の発⾏する学術雑誌 Foundations of Chemistry に 2020 年 4 ⽉ 21 ⽇に掲載されました。
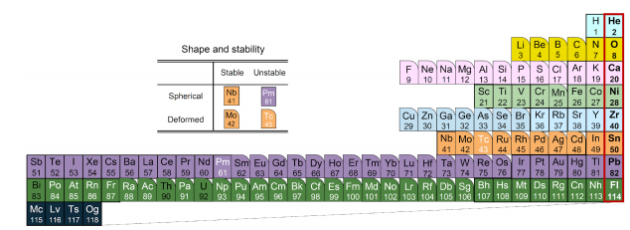
図1:新しい原⼦核の周期表1.背景
元素を構成する原⼦の中⼼には原⼦核があり、その周りを電⼦がまわっています(図2)。原⼦核に含まれる陽⼦の数が「原⼦番号」です。そして元素記号を原⼦番号の順に並べて、似た性質の元素が周期的に現れることを表現したのが「元素の周期表」です(図3)。昨年 2019 年は、メンデレーエフ(Dmitri Mendeleev)が元素周期律の発⾒に基づく周期表を発表してから 150 周年で、ユネスコ国際周期表年として世界中で活動が展開されました。現在、世界中でひろく使われている周期表は、実はメンデレーエフの考案した「短周期表」ではなく、ヴェルナー(Alfred Werner)が考案した「⻑周期表」に基づいています。
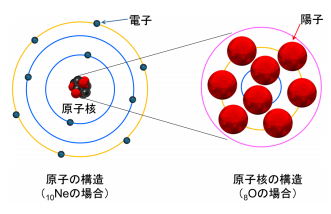
図2:原⼦と原⼦核の構造の模式図。原⼦核には陽⼦(⾚)と中性⼦(⿊)が詰まっています。例として、原⼦は希ガスの Ne(ネオン)の電⼦の軌道、原⼦核は魔法数を持つ O(酸素)の陽⼦の軌道を⽰します。また、それぞれの円は軌道の殻を表しています。
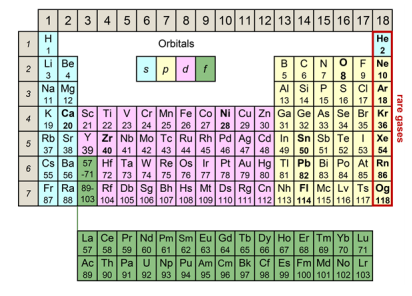
図3.元素の周期表(ヴェルナーの⻑周期表)
原⼦核は陽⼦の数に⽐例したプラスの電気をもっています。その周りをまわる電⼦がエネルギーの低い軌道から順番に詰まっていく様⼦を表現したのが元素の周期表です。図3の⾊は軌道の違いを表します。右端の列のヘリウム、ネオンなどは希ガスと呼ばれ、電⼦が軌道の殻をちょうど埋め尽くした状態にあるので、とても安定で化学反応を起こさない元素です。
実は、原⼦核そのものの中でも、それを構成する陽⼦や中性⼦に対して同様の軌道運動を考えることができます。原⼦核ではその中⼼にさらに別の「核」があるわけではありません。しかし、陽⼦や中性⼦にはたらく相互作⽤(湯川秀樹が考えた「核⼒」とよばれる強い相互作⽤)によって、電⼦のようにいくつかの殻に分かれた軌道ができ、エネルギーの低い軌道から順に詰まっていきます。これは原⼦核の殻模型(からもけい、シェルモデル)(注)と呼ばれます。魔法数の原⼦核は殻がちょうど埋まった原⼦核になり、希ガスに対応しています。しかし、電⼦と陽⼦・中性⼦とでは図2にあるように環境(ポテンシャル)が異なるので、各殻が収容できる最⼤の粒⼦数は原⼦の場合と原⼦核の場合で⼤きく異なります。軌道の殻が埋まって安定になるのは、原⼦の場合は電⼦の数が 2, 10, 18, 36, 54, 86 ですが、原⼦核の場合は陽⼦の数が 2, 8, 50, 82, 114 になるときです。また、陽⼦の数が 40 になるときにも程度は⼩さいものの同様の性質を⽰します。中性⼦にも同様の魔法数があり、114 の代わりに 126 になっている以外は陽⼦と同じ数になっています。
2.発想と成果
それでは、原⼦核の周期表は作れないものでしょうか? 原⼦核の中には陽⼦以外に中性⼦も含まれるので、同じ元素でも中性⼦の数の異なる同位体が存在します。中性⼦の数も原⼦核の安定性に⼤きく影響します。それらをすべて網羅した核図表は知られていますが、元素の周期表との対応性は⾒えません。
そこで、それぞれの元素に対して最も代表的な同位体を選ぶことで、冒頭の図1でご紹介した元素の周期表に対応する原⼦核の周期表を考案しました。右端には希ガスに対応して、陽⼦の数が魔法数となる元素が並んでいます。不思議なことにこのような原⼦核の周期表はこれまで知られておらず、世界で初めてとなります。
下の図4は、陽⼦の軌道殻を元素の周期表(図3)にならって⾊分けしたものです。原⼦の魔法数と原⼦核の魔法数の違いも視覚的にわかるようになっています。⻘い背景⾊は丸く広がった s 軌道(図2の⻘い円)を表します。3番⽬の 3s 軌道からなる殻が埋まるのは、電⼦では 12 番元素のマグネシウム(Mg)ですが、陽⼦では 70 番元素のイッテルビウム(Yb)となり、電⼦と陽⼦の軌道の性質の⼤きな違いが反映されています。
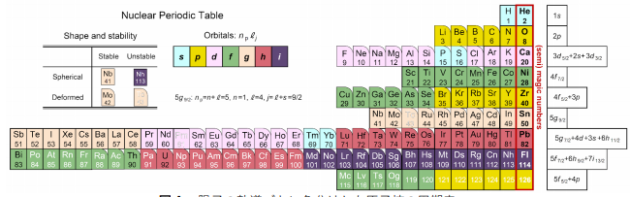
図4.陽⼦の軌道ごとに⾊分けした原⼦核の周期表
この周期表を⾒ると、魔法数を満たす安定な原⼦核は球形に近い形をしています。これに対して、魔法数から離れるほど、ラグビーボールのように変形した原⼦核(⾓の丸い箱)が多く、また鉛(Pb)より原⼦番号が⼩さくても⾃然崩壊してしまう不安定な原⼦核(⽩抜き元素記号)が出てきます。このように、この新
しい原⼦核の周期表では、殻構造だけでなく、それぞれの元素の原⼦核の変形や安定性も⼀⽬でわかります。
さらに、よく⽤いられる図 3 の原⼦の元素周期表に類似の形にしたものが図5です。ここで注意すべき⼤きな違いがあります。原⼦の周期表では、同じ列(族)に属する上下の元素は、同じ⾊で表したように同じ性質の軌道の電⼦をもつため性質に類似性があります。しかし原⼦核の周期表では、上で述べたような魔法数の周りでの性質の周期性はあるものの、⾊の違いから分かるように同じ列の上下では異なる軌道の陽⼦を持つため、それらの性質に特に類似性はありません。
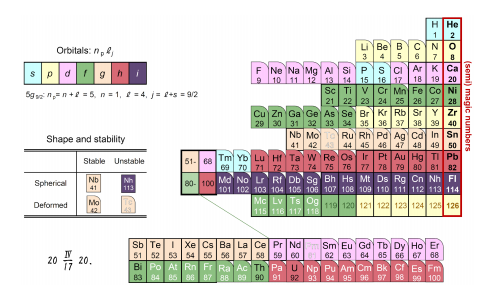
図5.元素の周期表(図3)と類似の形に整理した原⼦核の周期表
3.今後の展開
元素の周期表との⽐較が容易な原⼦核の周期表ができたことで、魔法数を含めて原⼦核の性質を学ぶ上での新しい指標ができます。今後は⼤学の教科書などにもこの原⼦核の周期表が掲載されて、教育に活⽤していただけるように願っています。
原⼦核の周期表は、⽴体的にもできます。図1(掲載論⽂の Fig. 2)を紙に印刷してはさみとセロテープの⼯作で下の写真(図6)のモデルが簡単に作れます。⽴体的な元素の周期表については、前野が約 20 年前に考案した「エレメンタッチ」が知られており、京都⼤学グッズとして販売もされています。これに対応して、原⼦核(nuclei、ニュークリアイ)の⽴体周期表は「ニュークリタッチ」と名付けました。

図6.原⼦核の⽴体周期表 ニュークリタッチ
4.⽀援を受けた研究プロジェクトについて
「国⺠との科学・技術対話」の活動にあたり、以下のプロジェクトからの⽀援を受けました。
・⽇本学術振興会 拠点形成事業(A: 先端拠点形成)(代表者:前野悦輝)(2017-2021 年度).
・⽇本学術振興会 科学研究費補助⾦・基盤S(代表者:前野悦輝)(2017-2021 年度、No. JP17H06136).
・⽇本学術振興会 新学術領域研究・計画研究(代表者:前野悦輝)(2015-2019 年度、No. JP15H05852).
<語句の説明>
(注)殻模型(からもけい、シェルモデル):核⼦が他の核⼦が作る平均的なポテンシャル(平均場)の中をそれぞれ独⽴に運動しているという観点から、1949 年、ゲッパート=メイヤーとイェンセンは独⽴に原⼦核の魔法数を説明することに成功しました。そこでは、強いスピン・軌道⼒が本質的な役割を果たしていることが⽰されました。この功績で 2 ⼈は 1963 年のノーベル物理学賞を受賞しました。これまで 3 名の⼥性がノーベル物理学賞を受賞しましたが、ゲッパート=メイヤーはその 2 番⽬でした。
<論⽂タイトルと著者>
タイトル:A Nuclear Periodic Table
著 者:Kouichi Hagino and Yoshiteru Maeno(萩野浩⼀,前野悦輝)掲 載 誌:Foundations of Chemistry
D O I:https://doi.org/10.1007/s10698-020-09365-5
(どなたでも無料でダウンロードできます。)