新しい電池が自動車、飛行機、トラックなどの動力源になる日が来るかもしれない New batteries could one day power cars, airplanes, trucks
2023-02-22 アルゴンヌ国立研究所(ANL)
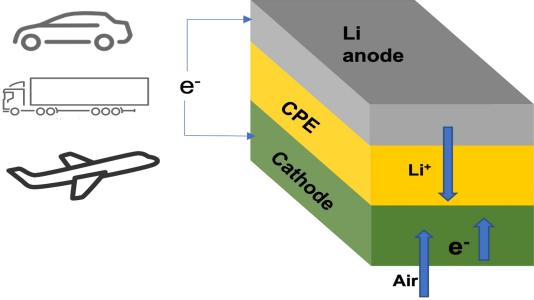
Schematic shows lithium-air battery cell consisting of lithium metal anode, air-based cathode, and solid ceramic polymer electrolyte (CPE). On discharge and charge, lithium ions (Li+) go from anode to cathode, then back. (Image by Argonne National Laboratory.)
◆電気自動車の所有者の多くは、1回の充電で1000マイル以上走行できるバッテリーパックを望んでいる。イリノイ工科大学(IIT)と米国エネルギー省(DOE)アルゴンヌ国立研究所の研究者らは、その夢を実現するリチウム空気電池を開発した。この新しい電池は、将来、国産飛行機や長距離トラックの動力源にもなりうるものです。
◆このリチウム空気電池の主な新要素は、通常の液体ではなく、固体電解質である。固体電解質は、リチウムイオン電池などに使われる液体電解質のように、過熱して発火するような安全上の問題がない。
◆さらに重要なのは、この固体電解質を用いた電池化学によって、リチウムイオン電池よりもエネルギー密度を4倍も高めることができる可能性があり、これは航続距離の延長につながるということである。
◆過去のリチウム空気電池の設計では、リチウム金属負極のリチウムが液体電解質中を移動して放電中に酸素と結合し、正極で過酸化リチウム(Li2O2)またはスーパーオキシド(LiO2)が生成されました。過酸化リチウムやスーパーオキシドは、充電時にリチウムと酸素の成分に分解される。この化学反応により、必要に応じてエネルギーが貯蔵・放出される。
◆「アルゴンヌの化学者ラシッド・アミネは、「過酸化リチウムの化学反応では、酸素1分子あたり1つか2つの電子が蓄えられるだけですが、酸化リチウムの場合は、4つの電子が蓄えられます。蓄えられる電子の数が多ければ多いほど、エネルギー密度が高くなります。
◆同チームが開発したリチウム空気電池は、室温で4電子反応を実現した最初のリチウム空気電池である。また、周囲の環境から供給される空気中の酸素で動作する。空気で動作することにより、従来の設計の問題点であった酸素ボンベの必要性を回避することができる。
◆研究チームは、4電子反応が実際に起こっていることを確認するために、さまざまな技術を採用した。その1つが、アルゴンヌのナノスケール材料センター(DOE Office of Scienceのユーザー施設)で行われた、カソード表面の放電生成物の透過電子顕微鏡観察(TEM)である。このTEM画像から、4電子放電のメカニズムについて貴重な知見が得られた。
◆これまでのリチウム空気電池は、サイクル寿命が非常に短いという欠点があった。研究チームは、1000サイクルの試験電池を製造・運転し、充電と放電の繰り返しに対する安定性を実証することで、この欠点が新しい設計の電池にはないことを確認した。
◆この研究は、サイエンスの最新号で発表されました。
<関連情報>
- https://www.anl.gov/article/new-design-for-lithiumair-battery-could-offer-much-longer-driving-range-compared-with-the-lithiumion
- https://www.science.org/doi/10.1126/science.abq1347
固体電解質を用いた室温充電可能なLi2O系リチウム空気電池を開発 A room temperature rechargeable Li2O-based lithium-air battery enabled by a solid electrolyte
Alireza Kondori ,Mohammadreza Esmaeilirad ,Ahmad Mosen Harzandi,Rachid Amine,Mahmoud Tamadoni Saray,Lei Yu,Tongchao Liu,Jianguo Wen,Nannan Shan,Hsien-Hau Wang,Anh T. Ngo,Paul C. Redfern,Christopher S. Johnson,Khalil Amine,Reza Shahbazian-Yassar,Larry A. Curtiss,Mohammad Asadi
Science Published:2 Feb 2023
DOI:https://doi.org/10.1126/science.abq1347
An enabling composite electrolyte
Lithium-air batteries have scope to compete with gasoline in terms of energy density. However, in most systems, the reaction pathways either involve one- or two-electron transfer, leading to lithium peroxide (Li2O2) or lithium superoxide (LiO2), respectively. Kondori et al. investigated a lithium-air battery that uses a ceramic-polyethylene oxide–based composite solid electrolyte and found that it can undergo a four-electron redox reaction through lithium oxide (Li2O) formation and decomposition (see the Perspective by Dong and Lu). The composite electrolyte embedded with Li10GeP2S12 nanoparticles shows high ionic conductivity and stability and high cycle stability through a four-electron transfer process. —MSL
Abstract
A lithium-air battery based on lithium oxide (Li2O) formation can theoretically deliver an energy density that is comparable to that of gasoline. Lithium oxide formation involves a four-electron reaction that is more difficult to achieve than the one- and two-electron reaction processes that result in lithium superoxide (LiO2) and lithium peroxide (Li2O2), respectively. By using a composite polymer electrolyte based on Li10GeP2S12 nanoparticles embedded in a modified polyethylene oxide polymer matrix, we found that Li2O is the main product in a room temperature solid-state lithium-air battery. The battery is rechargeable for 1000 cycles with a low polarization gap and can operate at high rates. The four-electron reaction is enabled by a mixed ion–electron-conducting discharge product and its interface with air.